Die molecular orbital (MO) Theorie ist ein Blick auf die Struktur des Moleküls durch die Verwendung von molekularen orbitalen gehören das Molekül als ganzes
anstatt zu den einzelnen Atomen. Wenn eine einfache Bindung zwischen zwei Atomen auftritt, nimmt das Elektronenpaar, das die Bindung bildet, ein MO ein, das eine mathematische Kombination der Wellenfunktionen der Atomorbitale der beiden beteiligten Atome darstellt. Die MO-Methode entstand in der Arbeit von Friedrich Hund und Robert S. Mulliken.
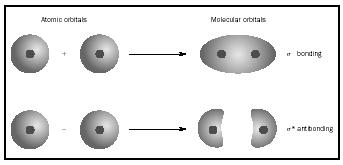
Wenn sich Atome zu einem Molekül verbinden, entspricht die Anzahl der Orbitale im Molekül der Anzahl der Orbitale in den kombinierenden Atomen. Wenn zwei sehr einfache Atome mit jeweils einem Atomorbital kombiniert werden, werden zwei molekulare Orbitale gebildet., Eines ist ein bindendes Orbital, dessen Energie niedriger ist als die Atomorbitale und von ihrer Summe abgeleitet ist. Es heißt Sigma. Der andere ist ein Antibonding-Orbital, dessen Energie höher ist als die Atomorbitale und sich aus ihrer Differenz ergibt. Es wird Sigma-1 ( σ*) genannt. (Siehe das Diagramm in Abbildung 1.)
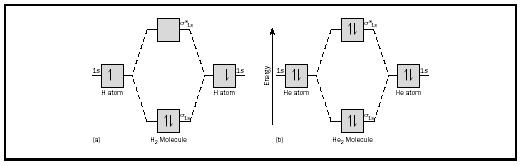
Die Grundidee könnte am besten durch die Betrachtung von zweiatomigen Molekülen von Wasserstoff und Helium veranschaulicht werden. Die Energiediagramme sind in Abbildung 2 dargestellt. Jedes Wasserstoffatom hat ein 1 s Elektron. Im H2-Molekül gehen die beiden Wasserstoffelektronen in die niedrigste verfügbare Energiequelle, das Sigma-Orbital., Im Fall von Helium hat jedes Heliumatom zwei Elektronen, so dass das he2-Molekül vier haben würde. Zwei würden in das untere Energiebindungs-Orbital gehen, aber die anderen beiden müssten in das höhere Energie-Sigma-Bindungs-Orbital gehen.
Bindungsreihenfolge
Die Bindungsreihenfolge für ein Molekül kann wie folgt bestimmt werden: Bindungsreihenfolge = ½ (Bindungselektronen − Bindungselektronen). Daher hat das H 2-Molekül eine Bindungsreihenfolge von ½ (2 − 0) = 1. Mit anderen Worten, es gibt eine einzige Bindung, die die beiden H-Atome im H 2-Molekül verbindet. Im Falle von He 2 hingegen ist die Bindungsreihenfolge ½ (2-2) = 0. Dies bedeutet, dass He 2 kein stabiles Molekül ist.,
Mehrfachbindungen
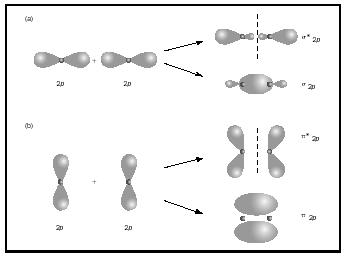
Doppel-oder Dreifachbindungen beinhalten zwei oder drei Paare von Bindungselektronen. Einzelne Bindungen sind immer Sigma-Bindungen, aber in mehreren Bindungen ist die erste Bindung Sigma, während jede zweite oder dritte Bindung Pi-Bindungen sind. Die Überlappung von p-Orbitalen kann entweder pi oder sigma MOs ergeben, wie in Abbildung 3 gezeigt. Wenn sie sich von Ende zu Ende überlappen, bilden sie Sigma-Orbitale, aber wenn sie sich Seite an Seite überlappen, bilden sie Pi-Orbitale.
Betrachten Sie jetzt das Sauerstoffmolekül., Die Lewis-Struktur für Sauerstoff ist: Ö:: Ö: Die Doppelbindung ist notwendig, um die Oktettregel für beide Sauerstoffatome zu erfüllen. Die gemessene Bindungslänge für Sauerstoff unterstützt das Vorhandensein einer Doppelbindung. Wir wissen jedoch, dass diese Lewis-Formel nicht die richtige Struktur für Sauerstoff sein kann, da Sauerstoff paramagnetisch ist, was bedeutet, dass das Sauerstoffmolekül ungepaarte Elektronen haben muss.
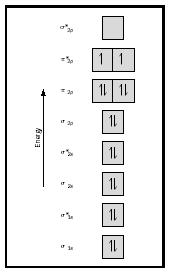
Schauen Sie sich nun das MO-Diagramm für Sauerstoff an, das in Abbildung 4 dargestellt ist. Es zeigt immer noch eine Bindungsreihenfolge von 2 an , zeigt aber auch zwei ungepaarte Elektronen.
Die MO-Theorie funktioniert auch gut für größere Moleküle wie N 2 O, CO 2 und BF 3 und für Ionen wie NO 3 − und CO 3 2− , bei denen die Bindungs-MOs delokalisiert sind und drei oder mehr Atome betreffen. Es ist besonders nützlich für aromatische matic Moleküle wie Benzol. In diesem Fall sind alle sechs C-Atome im Ring gleichermaßen an einer delokalisierten pi-Elektronenwolke beteiligt, die das gesamte Molekül umhüllt., Die MO-Theorie kann sogar auf komplexe Ionen und Feststoffe ausgedehnt werden, einschließlich Materialien wie Supraleitern und Halbleitern.