Siehe unseren vorherigen Beitrag zu den 6 wichtigen EAS-Reaktionen, die Sie für das DAT kennen müssen.
Jetzt müssen wir uns auf Benzolsubstituenten konzentrieren und wie sie den Ort nachfolgender Zusätze beeinflussen., Hier ist eine Liste der, die Sie höchstwahrscheinlich sehen würden:
Elektronenspender / Aktivatoren (am stärksten bis am schwächsten): -O–,- NR2,- NH2,- OH,- ODER-R
Elektronenentnahme / – deaktivierer (am stärksten bis am schwächsten):- NO2,- NR3+,- NH3+,- SO3H,- CN,- CO2H,- CO2R,- COH, – X (Halogene)
Allgemein gesprochen, Elektronenspender / Aktivatoren haben ein einsames Elektronenpaar oder eine Elektronendichte, die in das Benzol „drückt“. Elektronenabzieher / – deaktivierer haben eine positive Ladung auf dem Substituenten oder ein sehr elektronegatives Atom, das daran befestigt ist und Elektronen aus dem Benzol“ zieht“.,
– Alle Aktivatoren sind ortho-para-Direktoren.
– Deaktivatoren (Halogene) sind Ortho-Para-Regie.
– Deaktivatoren (nicht Halogene) sind Meta-Regie.
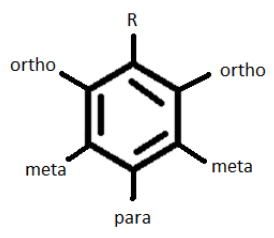
Daher würde je nach Zeichen des ursprünglichen Substituenten (R) ein nachfolgender Substituent an der Ortho-oder Para-Position platziert, wenn R ein Aktivator/Halogen ist, oder an der Metaposition, wenn es sich um einen Deaktivierer (aber kein Halogen) handelt.,
Weitere Fakten zu wissen:
- Je mehr Elektronenspendergruppen ein Benzolring anfangs hat, desto schneller tritt eine EAS-Reaktion auf (aufgrund der erhöhten Elektronendichte, um Benzol zu einem besseren Nukleophilen zu machen).
- Wenn sich bereits zwei oder mehr Substituenten auf dem Ring befinden, erhält die stärkste Spendergruppe Priorität bei der Auswahl des Ortes des hinzugefügten Substituenten.
- Bei einer Ortho / Para-Wahl gehen Substituenten mit dem geringsten sterischen Stamm an den Ort.