Introduction
Alkenes and alkynes are hydrocarbons which respectively have carbon-carbon double bond and carbon-carbon triple bond functional groups. As fórmulas moleculares destes hidrocarbonetos insaturados refletem a ligação múltipla dos grupos funcionais:
alcenos são nomeados como se fossem alcanos, mas o sufixo “-ane” é alterado para “-Eno”., Se o alceno contém apenas uma ligação dupla e essa ligação dupla é terminal (a ligação dupla está numa extremidade da molécula ou outra), então não é necessário colocar nenhum número na frente do nome.,
butano: C4H10 (CH3CH2CH2CH3)
buteno: C4H8 (CH2=CHCH2CH3)
Se a ligação dupla não é de terminal (se ele estiver em um de carbono em algum lugar no centro da cadeia) em seguida, os carbonos devem ser numeradas de forma a dar a primeira das duas ligada carbonos o menor número possível, e esse número deve preceder o “ene” sufixo com um traço, como mostrado abaixo.,
correto: pent-2-eno (CH3CH=CHCH2CH3)
incorreta: pent-3-eno (CH3CH2CH=CHCH3)
A segunda é incorreta porque, lançando a fórmula na horizontal resulta em um número menor para o alkene.
Se houver mais de uma ligação dupla num alceno, todas as ligações devem ser numeradas em nome das ligações duplas terminais par – moléculas. Os números devem ir do mais baixo para o mais alto, e ser separados um do outro por uma vírgula. Os prefixos numéricos IUPAC são usados para indicar o número de ligações duplas.,
octa-2,4-dieno: CH3CH=CHCH=CHCH2CH2CH3
deca-1,5-dieno: CH2=CHCH2CH2CH=CHCH2CH2CH2CH3
Note que a numeração das “2-4” acima produz uma molécula com duas ligações duplas separadas por apenas um título único. Ligações duplas em tal condição são chamadas de “conjugadas”, e elas representam uma estabilidade melhorada de conformação, então elas são energeticamente favorecidas como reagentes em muitas situações e combinações.,
| alcano | CnH2n+2 | esta é a razão H / C máxima para um dado número de átomos de carbono.cada ligação dupla reduz o número de átomos de hidrogénio em 2. |
|---|
A estrutura principal é a cadeia mais longa que contém ambos os átomos de carbono da ligação dupla., Os dois átomos de carbono da ligação dupla e os quatro átomos ligados a eles se encontram em um avião, com ângulos de ligação de aproximadamente 120° Uma ligação dupla consiste de um sigma vínculo formado pela sobreposição sp2 híbrido orbitais e um pi vínculo formado pela sobreposição de paralelo 2 orbitais p
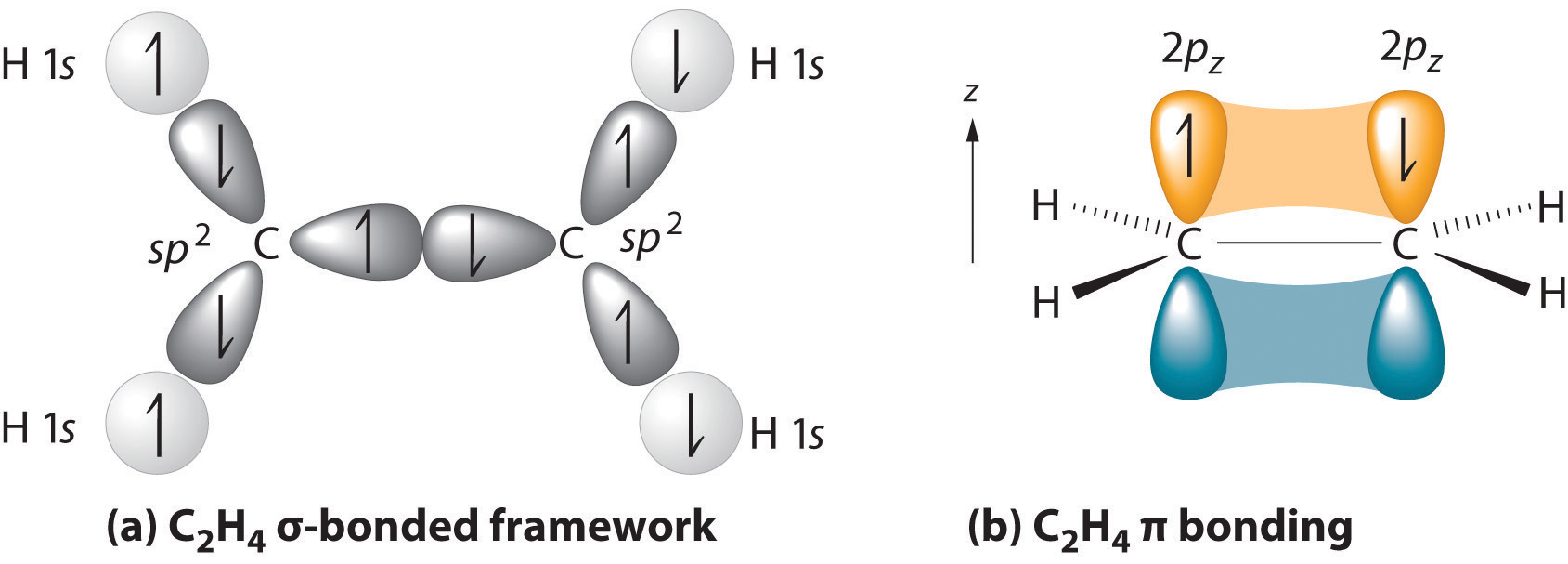
A fórmula molecular de um hidrocarboneto fornece informações sobre os possíveis tipos estruturais ele pode representar. Por exemplo, considere compostos com a fórmula C5H8., A fórmula do alquano pentano de cinco carbonos é C5H12 de modo que a diferença no teor de hidrogênio é 4. Esta diferença sugere que tais compostos podem ter uma ligação tripla, duas ligações duplas, um anel mais uma ligação dupla, ou dois anéis. Alguns exemplos são mostrados aqui, e há pelo menos quatorze outros!