Richard Baxter und Jim Britton
Wie korrodiert Stahl im Wasser?
Um den kathodischen Schutz zu verstehen, müssen Sie zuerst verstehen, wie Korrosion verursacht wird. Damit Korrosion auftreten kann, müssen drei Dinge vorhanden sein:
1. Zwei unähnliche Metalle
2. Ein Elektrolyt (Wasser mit jeder Art von Salz oder darin gelösten Salzen)
3., Ein Metall (leitender) Weg zwischen den unähnlichen Metallen
Die beiden unähnlichen Metalle können völlig unterschiedliche Legierungen sein – wie Stahl und Aluminium–, sind jedoch eher mikroskopische oder makroskopische metallurgische Unterschiede auf der Oberfläche eines einzelnen Stahlstücks. In diesem Fall betrachten wir korrosionsfreien Stahl, der ungleichmäßig ist.
Wenn die oben genannten Bedingungen vorliegen, findet die folgende Reaktion an den aktiveren Stellen statt: (zwei Eisenionen plus vier freie Elektronen).,
2Fe => 2Fe++ + 4e –
Die freien Elektronen wandern durch den Metallweg zu den weniger aktiven Stellen, wo die folgende Reaktion stattfindet: (Sauerstoffgas wird in Sauerstoffion umgewandelt – durch Kombination mit den vier freien Elektronen-die sich mit Wasser zu Hydroxylionen verbinden).
O2 + 4e – + 2H20 => 4 OH-
Rekombinationen dieser Ionen an der aktiven Oberfläche erzeugen die folgende Reaktion, die das Eisen-Korrosions-Produkt Eisenhydroxid ergibt: (Eisen kombiniert mit Sauerstoff und Wasser zu Eisenhydroxid).,
2Fe + O2 + 2H2O = 2Fe (OH)2
Diese Reaktion wird häufiger als ‚Stromfluss durch das Wasser von der Anode (aktivere Stelle) zur Kathode (weniger aktive Stelle) beschrieben.‘
Wie stoppt der kathodische Schutz die Korrosion?
Der kathodische Schutz verhindert Korrosion, indem alle anodischen (aktiven) Stellen auf der Metalloberfläche in kathodische (passive) Stellen umgewandelt werden, indem elektrischer Strom (oder freie Elektronen) aus einer alternativen Quelle zugeführt wird.
Normalerweise hat dies die Form von galvanischen Anoden, die aktiver sind als Stahl., Diese Praxis wird auch als Opfersystem bezeichnet, da sich die galvanischen Anoden opfern, um den Baustahl oder die Rohrleitung vor Korrosion zu schützen.
Bei Aluminiumanoden ist die Reaktion an der Aluminiumoberfläche: (vier Aluminiumionen plus zwölf freie Elektronen)
4Al => 4AL+++ + 12 e –
und an der Stahloberfläche: (Sauerstoffgas, das in Sauerstoffionen umgewandelt wird, die sich mit Wasser zu Hydroxylionen verbinden).,
3O2 + 12e – + 6H20 => 12OH-
Solange der Strom (freie Elektronen) schneller als Sauerstoff an der Kathode (Stahl) ankommt, tritt keine Korrosion auf.,
Grundlegende Überlegungen beim Entwurf von Opferanodensystemen
Der elektrische Strom, den eine Anode entlädt, wird durch das Ohmsche Gesetz gesteuert, das lautet:
I=E/R
I= Stromfluss in Ampere
E= Potentialdifferenz zwischen Anode und Kathode in Volt
R= Gesamtkreiswiderstand in Ohm
Anfänglich ist der Strom hoch, da die Potentialdifferenz zwischen Anode und Kathode hoch ist.hoch, aber wenn die Potentialdifferenz aufgrund der Wirkung des Stromflusses auf die Kathode abnimmt, nimmt der Strom aufgrund der Polarisation der Kathode allmählich ab., Der Schaltungswiderstand umfasst sowohl den Wasserweg als auch den Metallpfad, der jedes Kabel in der Schaltung enthält. Der dominierende Wert ist hier der Widerstand der Anode gegen das Meerwasser.
Für die meisten Anwendungen ist der Metallwiderstand im Vergleich zur Wasserbeständigkeit so gering, dass er ignoriert werden kann (obwohl dies nicht für Schlitten oder lange Rohrleitungen gilt, die an beiden Enden geschützt sind). Im Allgemeinen haben lange, dünne Anoden einen geringeren Widerstand als kurze, fette Anoden. Sie entladen mehr Strom, halten aber nicht so lange.,
Daher muss ein Kathodenschutzdesigner die Anoden so dimensionieren, dass sie die richtige Form und Oberfläche haben, um genügend Strom zu entladen, um die Struktur zu schützen, und genügend Gewicht, um die gewünschte Lebensdauer beim Entladen dieses Stroms zu erreichen.
Als allgemeine Faustregel gilt:
Die Länge der Anode bestimmt, wie viel Strom die Anode erzeugen kann und folglich wie viele Quadratfuß Stahl geschützt werden können. Der Querschnitt (Gewicht) bestimmt, wie lange die Anode dieses Schutzniveau aufrechterhalten kann.,
Hochstromkathodische Schutzsysteme (ICCP-Anodensysteme)
Aufgrund der hohen Ströme in vielen Meerwassersystemen ist es nicht ungewöhnlich, Hochstromsysteme zu verwenden, die Anoden eines Typs (ICCP-Anoden) verwenden, die sich nicht leicht in Metallionen lösen lassen. Dies verursacht eine alternative Reaktion: die Oxidation der gelösten Chloridionen.
2Cl – = Cl2 + 2e-
Die Stromversorgung erfolgt über ein externes Gleichstromaggregat.,

Woher wissen wir, wann wir genug kathodischen Schutz haben?
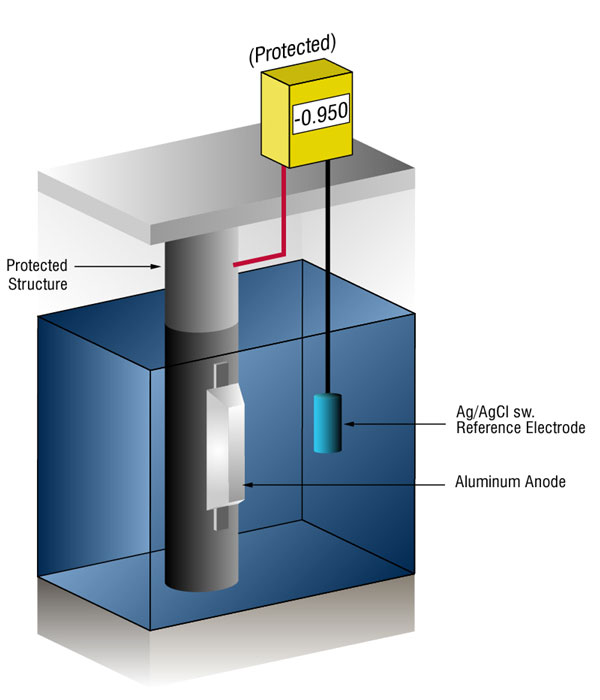
Wir können überprüfen, ob genügend Strom vorhanden ist, indem wir das Potential des Stahls gegen eine Standardreferenzelektrode messen, normalerweise Silbersilber / Chlorid (Ag/AgCl sw.), aber manchmal Zink (sw.).
Der Stromfluss auf jedes Metall verschiebt sein normales Potential in die negative Richtung. Die Geschichte hat gezeigt, dass, wenn Stahl genug Strom erhält, um das Potenzial auf (-) 0,800 V zu verschieben vs., silver / silver chloride (Ag / AgCl), the corrosion is essentially stopped.
 |
 |