Einleitung
Alkene und Alkine sind Kohlenwasserstoffe, die jeweils Kohlenstoff-Kohlenstoff-Doppelbindung und Kohlenstoff-Kohlenstoff-Dreifachbindung funktionelle Gruppen haben. Die molekularen Formeln dieser ungesättigten Kohlenwasserstoffe spiegeln die Mehrfachbindung der funktionellen Gruppen wider:
Alkene werden so benannt, als wären sie Alkane, aber das Suffix „-ane“ wird in „-ene“geändert., Wenn das Alken nur eine Doppelbindung enthält und diese Doppelbindung terminal ist (die Doppelbindung befindet sich an einem Ende des Moleküls oder eines anderen Moleküls), ist es nicht erforderlich, eine Zahl vor den Namen zu setzen.,
Butan: C4H10 (CH3CH2CH2CH3)
Buten: C4H8 (CH2=CHCH2CH3)
Wenn die Doppelbindung nicht terminal ist (wenn sie sich irgendwo in der Mitte der Kette auf einem Kohlenstoff befindet), sollten die Kohlenstoffe so nummeriert sein, dass die erste der beiden Doppel-gebundene Kohlensäure die niedrigstmögliche Zahl, und diese Zahl sollte dem Suffix „ene“ mit einem Bindestrich vorangestellt sein, wie unten gezeigt.,
richtig: pent-2-ene (CH3CH=CHCH2CH3)
falsch: pent-3-ene (CH3CH2CH=CHCH3)
Die zweite ist falsch, weil du die Formel horizontal Ergebnisse in eine niedrigere Zahl für das Alken.
Wenn mehr als eine Doppelbindung in einem Alken vorhanden ist, sollten alle Bindungen im Namen des Moleküls nummeriert sein – auch terminale Doppelbindungen. Die Zahlen sollten vom niedrigsten zum höchsten gehen und durch ein Komma voneinander getrennt sein. Die numerischen IUPAC-Präfixe werden verwendet, um die Anzahl der Doppelbindungen anzugeben.,
– octa-2,4-dien: CH3CH=CHCH=CHCH2CH2CH3
deca-1,5-dien: CH2=CHCH2CH2CH=CHCH2CH2CH2CH3
Beachten Sie, dass die Nummerierung der „2-4“ oben ergibt sich ein Molekül mit zwei Doppelbindungen voneinander getrennt durch nur eine Einfachbindung. Doppelbindungen in einem solchen Zustand werden als „konjugiert“ bezeichnet und stellen eine verbesserte Stabilität der Konformation dar, so dass sie in vielen Situationen und Kombinationen als Reaktanten energetisch bevorzugt werden.,
| Alkan | CnH2n+2 | Dies ist das maximale H/C-Verhältnis für eine bestimmte Anzahl von Kohlenstoffatomen. |
|---|---|---|
| Alken | CnH2n | Jede Doppelbindung reduziert die Anzahl der Wasserstoffatome um 2. |
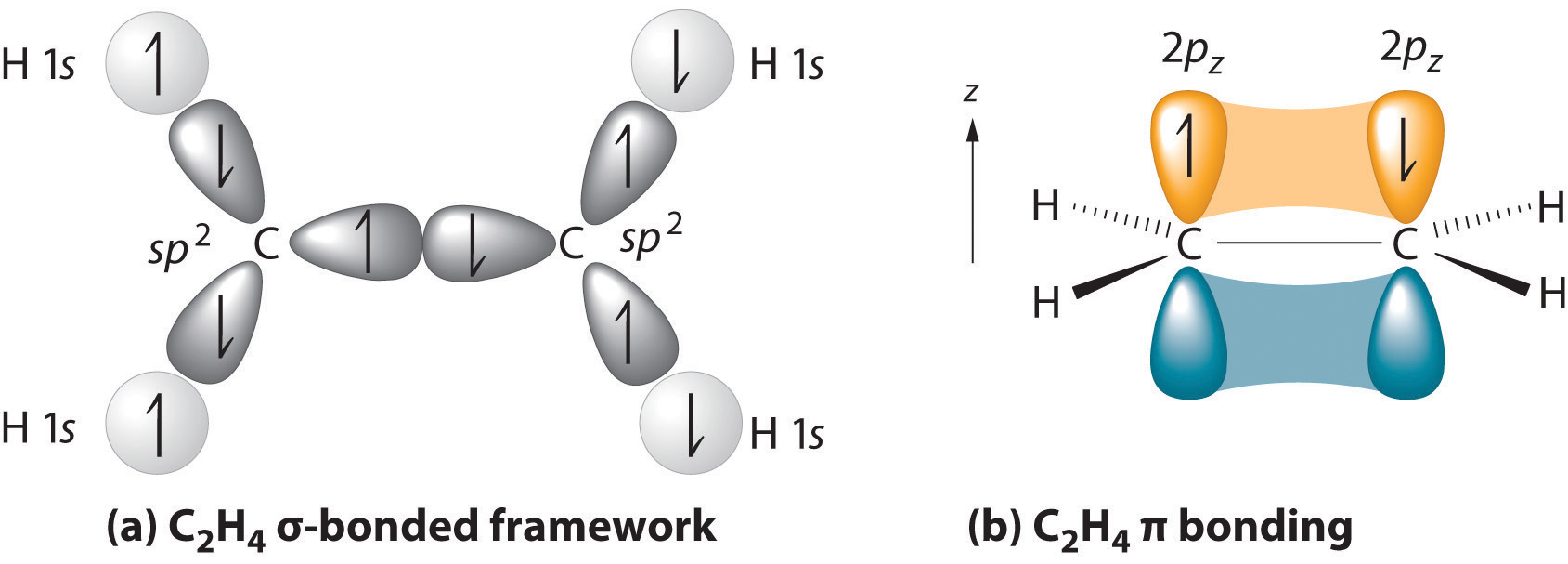
Die übergeordnete Struktur ist die längste Kette, die beide Kohlenstoffatome der Doppelbindung enthält., Die beiden Kohlenstoffatome einer Doppelbindung und die vier Atome, die an ihnen befestigt sind, liegen in einer Ebene, mit Bindungswinkeln von ungefähr 120° Eine Doppelbindung besteht aus einer Sigma-Bindung, die durch Überlappung von sp2-Hybridbahnen gebildet wird, und einer pi-Bindung, die durch Überlappung paralleler 2 p-Orbitale gebildet wird
Die Molekülformel eines Kohlenwasserstoffs liefert Informationen über die möglichen Strukturtypen, die er darstellen kann. Betrachten Sie beispielsweise Verbindungen mit der Formel C5H8., Die Formel des Fünf-Kohlenstoff-Alkan-Pentans ist C5H12, so dass der Unterschied im Wasserstoffgehalt 4 beträgt. Dieser Unterschied deutet darauf hin, dass solche Verbindungen eine Dreifachbindung, zwei Doppelbindungen, einen Ring plus eine Doppelbindung oder zwei Ringe haben können. Einige Beispiele werden hier gezeigt, und es gibt mindestens vierzehn andere!