wprowadzenie
stężenie jest miarą ilości danej substancji zmieszanej z inną substancją. Mówi się, że roztwory są rozcieńczane lub zagęszczane. Kiedy mówimy, że ocet jest \(5\%\) kwasem octowym w wodzie, podajemy stężenie. Gdybyśmy powiedzieli, że mieszanina jest \(10\%\) kwas octowy, byłoby to bardziej skoncentrowane niż roztwór octu.,
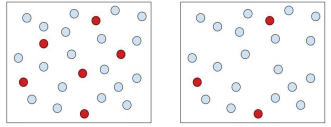
stężony roztwór to taki, w którym w danej ilości rozpuszczalnika znajduje się duża ilość substancji rozpuszczonej., Rozcieńczony roztwór to taki, w którym znajduje się niewielka ilość substancji rozpuszczonej w danej ilości rozpuszczalnika. Rozcieńczony roztwór jest stężonym roztworem, który został zasadniczo rozcieńczony. Pomyśl o pojemnikach na mrożone soki, które kupisz w sklepie spożywczym. Aby zrobić sok, musisz wymieszać koncentrat mrożonego soku z wnętrza tych pojemników z trzy lub cztery razy większym pojemnikiem pełnym wody. Dlatego rozcieńczasz skoncentrowany sok. Pod względem substancji rozpuszczonej i rozpuszczalnika, stężony roztwór ma dużo substancji rozpuszczonej w porównaniu do rozcieńczonego roztworu, który miałby mniejszą ilość substancji rozpuszczonej.,
terminy „skoncentrowany” i „rozcieńczony” dostarczają jakościowych metod opisywania stężenia. Chociaż obserwacje jakościowe są niezbędne i mają swoje miejsce w każdej części nauki, w tym w chemii, widzieliśmy w trakcie naszych badań naukowych, że istnieje wyraźna potrzeba pomiarów ilościowych w nauce. Jest to szczególnie prawdziwe w chemii roztworów. W tej sekcji przyjrzymy się kilku ilościowym metodom wyrażania stężenia roztworu.