Introduzione
Tuttavia, diversi studi sugli animali hanno dimostrato che il CBD produce curve dose-risposta a forma di U invertite. Queste curve sono state descritte per la prima volta nei ratti testati nel modello di ansia elevated plus maze (EPM) (Guimarães et al., 1990). In quello studio, il CBD ha aumentato l’esplorazione a braccio aperto (un effetto simile all’ansiolitico) a dosi di 2,5–10 mg/kg, ma non a 20 mg/Kg (Guimarães et al., 1990)., Simili curve dose-risposta a forma di campana sono state descritte in altri studi che studiano gli effetti comportamentali del CBD. Ad esempio, il pesce zebra trattato con 0,5 mg/kg di CBD ha trascorso molto più tempo nella zona superiore dell’acquario (che viene interpretato come un effetto simile all’ansiolitico), mentre il comportamento dei pesci trattati con il più basso (0,1 mg/kg) e le dosi più alte (5 e 10 mg/kg) non differiva dai controlli (Nazario et al., 2015). Un modello simile è stato osservato anche nei ratti spontaneamente ipertesi (SHRs), che presentano un fenotipo comportamentale simile alla schizofrenia., L’inibizione prepulse in questo ceppo di ratti è stata invertita da 30 mg / kg di CBD, ma non dalle dosi di 15 e 60 mg / kg (Levin et al., 2014). Lo stesso è stato osservato utilizzando il modello di compromissione cognitiva indotta da reserpina nei ratti, un modello animale sia della malattia di Parkinson che della discinesia tardiva. Mentre il CBD, alla dose di 0,5 mg/kg, ha attenuato il deficit di memoria indotto dalla reserpina nel compito discriminativo, la dose di 5 mg / kg si è dimostrata inefficace (Peres et al., 2016).,
C’è una chiara necessità di esplorare nuovi modi di gestire i disturbi d’ansia, poiché il loro trattamento rimane problematico e di solito comporta una combinazione di farmaci, tra cui benzodiazepine e antidepressivi. Questi farmaci hanno i loro svantaggi come il rischio di dipendenza e sindrome da astinenza, effetti collaterali sessuali, compromissione cognitiva e psicomotoria, insorgenza ritardata dell’azione (antidepressivi), bassa accettazione e requisito di un attento controllo del dosaggio (Katzman et al., 2014; Bandelow et al., 2015; Sgnaolin et al., 2016)., Il CBD non sembra indurre effetti avversi significativi nell’uomo (Bergamaschi et al., 2011b). Tuttavia, da una possibile prospettiva terapeutica, è essenziale determinare se un modello di dose-risposta simile a forma di U invertita è presente anche negli esseri umani. Per indagare questa possibilità, abbiamo scelto uno degli effetti più consistenti del CBD, la diminuzione acuta dell’ansia. Questo effetto è stato descritto in diversi modelli animali e in volontari sani e pazienti con disturbo d’ansia sociale (SAD) (Guimarães et al., 1990; Zuardi et al., 1993; Bergamaschi et al., 2011a; Crippa et al.,, 2011); tuttavia, non è stato studiato utilizzando dosi multiple negli esseri umani.
Un metodo ampiamente utilizzato per indurre l’ansia sperimentale negli esseri umani è il compito di parlare in pubblico simulato (SPST – Graeff et al., 2003). L’SPST è molto coerente nell’elevare l’ansia auto-valutata. Tuttavia, i suoi effetti sulle risposte fisiologiche (frequenza cardiaca, pressione sanguigna e secrezione di cortisolo) sono meno consistenti (Palma et al., 1994; Hetem et al., 1996; de-Paris et al., 2003)., Una meta-analisi di 11 studi che hanno utilizzato l’SPST ha confermato questa osservazione, mostrando un aumento significativo della dimensione complessiva dell’effetto sull’ansia soggettiva, ma non sulla pressione arteriosa sistolica (SBP) e sulla frequenza cardiaca (Zuardi et al., 2013). Scarse prove in letteratura suggeriscono che parlare in pubblico in una situazione di vita reale è più efficiente per aumentare le risposte fisiologiche (Turner et al., 1990; Dickerson e Kemeny, 2004). In un recente studio, abbiamo confrontato il test di parlare in pubblico in una situazione reale (TPSRS) e l’SPST., I risultati hanno mostrato che entrambi i metodi erano efficaci nell’aumentare l’ansia soggettiva, ma solo il TPSRS aumentava la frequenza cardiaca, la SBP e la pressione diastolica (DBP) (Zuardi et al., 2013).
Il presente studio, pertanto, è stato progettato per testare l’ipotesi che l’aumento delle dosi di CBD produrrebbe effetti ansiolitici in un modello di dose-risposta a forma di U invertita in volontari sani sottoposti al TPSRS.,
Materiali e metodi
Soggetti
Sessanta uomini e donne sani di età compresa tra 18 e 35 anni, senza storia di malattie psichiatriche passate o attuali, alcol o altre tossicodipendenze sono stati reclutati attraverso la pubblicità nel campus dell’Università di São Paulo a Ribeirão Preto. I partecipanti con condizioni mediche importanti o che stavano assumendo farmaci con il potenziale di interferire con i risultati dello studio non sono stati inclusi., I volontari sono stati intervistati al fine di valutare l’ammissibilità e misurare la loro propensione all’ansia attraverso la versione tratto dello Spielberger State-Trait Anxiety Inventory (STAI – Spielberger et al., 1970). I partecipanti idonei che hanno accettato di partecipare sono stati istruiti ad astenersi dai farmaci nella settimana prima dei test e da alcol e caffeina nel 24 h prima del test., Tutti i volontari hanno dato il consenso informato scritto a partecipare dopo essere stati pienamente informati delle procedure di ricerca, conformi agli attuali termini della Dichiarazione di Helsinki e sono stati approvati dal Comitato Etico dell’Ospedale universitario Ribeirão Preto Medical School (HCRP-No. 12407/09).
I volontari sono stati assegnati in modo casuale a cinque gruppi con 12 soggetti ciascuno per ricevere diverse dosi di CBD (100, 300 e 900 mg), clonazepam (1 mg) o placebo in un design randomizzato in doppio cieco., I gruppi sono stati abbinati in base al sesso, all’età, all’indice di massa corporea (BMI) e al punteggio STAI-trait. Un volontario del gruppo CBD – 300 non ha potuto partecipare alla sessione sperimentale a causa di problemi personali ed è stato ritirato dallo studio.
Farmaci
La polvere di cannabidiolo con purezza del 99,6% (nessun altro cannabinoide presente) disciolta in olio di mais a dosi di 100 e 200 mg / ml è stata gentilmente fornita da Biosynthesis Pharma Group (BSPG-Pharm, Sandwich, UK). La soluzione di CBD, le compresse di clonazepam (Rivotril®, Roche Lab) e placebo (olio di mais) erano confezionate in capsule di gelatina identiche., Tutti i volontari hanno ricevuto cinque capsule di un millilitro di ciascuno, nelle seguenti combinazioni: cinque capsule contenenti olio di mais (gruppo placebo); una capsule di CBD 100 mg/ml e quattro capsule di olio di mais (CBD-100 gruppo); tre capsule di CBD 100 mg/ml e due capsule di olio di mais (CBD-300 di gruppo); quattro capsule di CBD 200 mg/ml e una capsula di CBD 100 mg/ml (CBD-900 gruppo); e una capsula con clonazepam e quattro capsule di olio di mais (clonazepam gruppo – CLONE)., Ogni trattamento ha ricevuto un numero casuale e sia lo sperimentatore incaricato di dispensare le capsule che il volontario non erano a conoscenza del loro contenuto (in doppio cieco). Infine, la scelta dell’intervallo tra la somministrazione del farmaco e il TPSRS si è basata su precedenti studi farmacologici che dimostrano che le concentrazioni plasmatiche di picco di CBD e CLON assunti per via orale di solito si verificano tra 2 e 3 h dopo l’ingestione (Agurell et al., 1981; Crevoisier et al., 2003; Borgwardt et al., 2008; Fusar-Poli et al., 2009; Martin-Santos et al., 2012)., Il CBD subisce un significativo effetto di primo passaggio che porta alla formazione di un certo numero di metaboliti e la sua emivita nell’uomo è risultata compresa tra 2 e 5 giorni dopo la somministrazione orale. La biodisponibilità del CBD orale negli esseri umani è di circa il 6%, sostenendo così l’opinione che abbia un sostanziale effetto di primo passaggio (Zhornitsky e Potvin, 2012). I livelli plasmatici medi di CBD a 1, 2 e 3 h dopo la somministrazione acuta di 600 mg erano rispettivamente 0,36, 1,62 e 3,4 ng/ml (Martin-Santos et al., 2012)., La scelta delle dosi utilizzate in questo studio si è basata su precedenti prove che dimostravano che la somministrazione orale acuta di 300 mg di CBD aveva effetti ansiolitici nel SPST (Zuardi et al., 1993).
Misure psicologiche
Due fattori della Visual Analog Mood Scale (VAMS), tradotti e validati in portoghese da Zuardi e Karniol (1981), sono stati utilizzati per valutare i livelli di ansia e gli effetti sedativi durante il test. Il VAMS è uno strumento auto-somministrato composto da 16 elementi. Prima del TPSRS, ogni volontario ha subito una sessione di formazione per completare la scala., Ai soggetti è stato chiesto di segnare il punto che ha identificato il suo stato soggettivo attuale su una linea retta di 100 mm posta tra due parole che descrivono stati d’animo opposti (ad esempio, rilassato-teso). Un’analisi fattoriale della versione portoghese della scala ha identificato quattro fattori (Zuardi et al.,, 1993): (1) ‘ansia’ composto da elementi calma–eccitato, rilassato–teso, e tranquilla, turbato; (2) ‘sedazione’, tra cui gli elementi di allarme–sonnolenza attento e sognante; (3) ‘cognitivo’, tra cui arguto, mentalmente lento, abile incompetente, energico in letargo, chiaro–muzzy, gregario–ritirata, ben coordinato–goffo, e forte–debole; e (4) il fastidio e ’ compreso l’voci interessate–annoiato, felice, triste, contento–scontenti, e amichevole–antagonisti (Parente et al., 2005). Da precedenti studi con entrambi ansiogeni (Crippa et al., 2004; Parente et al.,, 2005) e farmaci ansiolitici tra cui CBD (Crippa et al., 2004, 2011; Bergamaschi et al., 2011a) hanno dimostrato che solo i fattori di ansia e sedazione presentano cambiamenti durante le attività di parlare in pubblico, abbiamo usato solo gli elementi di questi fattori delle VAMS per ridurre i tempi di somministrazione e consentire l’esecuzione del protocollo. Questa procedura è stata utilizzata in precedenza nello studio di validazione del PSRST (Zuardi et al., 2013).
Misurazioni fisiologiche
La pressione arteriosa sistolica, DBP e frequenza cardiaca (HR) sono state misurate con uno sfigmomanometro digitale (Omron, Brasile).,
Test di Public Speaking in a Real Situation (TPSRS)
In questa procedura, ogni soggetto deve parlare di fronte a un gruppo e, nella stessa sessione sperimentale, partecipare al pubblico quando gli altri membri del gruppo stanno parlando. Il pubblico è incaricato di rimanere in silenzio e con un’espressione neutra durante i discorsi.
Sono state effettuate cinque sessioni sperimentali con 12 soggetti ciascuna (tranne 1, che comprendeva 11 soggetti). All’inizio della sessione, i volontari sono stati informati del numero del trattamento che avrebbero ricevuto (come descritto sopra)., I volontari sono stati quindi istruiti a prendere posti contrassegnati con i rispettivi numeri di trattamento. I posti erano numerati in modo tale che, al termine delle cinque sessioni, i soggetti di ciascun gruppo di trattamento avessero occupato tutte le posizioni possibili. La sequenza di procedure ha sempre seguito lo stesso ordine dalla prima alla dodicesima sedia nel tentativo di minimizzare un possibile effetto di ordine nella sequenza degli altoparlanti., Ad esempio, i soggetti del gruppo CBD-300 occupavano le seguenti posizioni: prima sessione – 3, 8; seconda sessione – 4, 9; terza sessione – 5, 10; quarta sessione – 1, 6, 11; quinta sessione – 2, 7, 12.
Procedura
I volontari hanno iniziato la sessione sperimentale dopo un minimo di 6 ore di sonno e 2 ore dopo aver mangiato una colazione standard (200 ml di latte al cioccolato e 100 g di pane con margarina).,
I 12 volontari sedevano su sedie disposte a semicerchio, seguendo un ordine predeterminato dal numero di trattamento assegnato a ciascuno di loro ed eseguivano le misurazioni di base, seguite dall’assunzione delle cinque capsule entro un intervallo di 5 minuti per ogni volontario. Questa fase è stata completata per un periodo di 1 h. I volontari hanno poi guardato un film sugli uccelli della foresta amazzonica della durata di circa 20 min. Successivamente, le misurazioni sono state ripetute con un intervallo di 5 min per ciascun soggetto (misura pre-test)., 2 h e 20 min dopo che il primo volontario aveva ricevuto il trattamento, tutti hanno guardato un video della durata di circa 10 min con le istruzioni registrate per il test vocale. 2 h e 30 min dopo che il primo volontario ha ricevuto il trattamento, hanno iniziato a eseguire il test vocale, che è durato 5 min. Successivamente, gli altri volontari sono stati sottoposti al test del linguaggio nello stesso ordine in cui avevano ricevuto i trattamenti., Il test vocale consisteva nel preparare silenziosamente un discorso di 1 minuto su un tema relativo alle ” condizioni di un servizio pubblico della tua città”, scelto per caso tra le opzioni 12 e rivelato immediatamente prima della preparazione del discorso. Il discorso preparato è stato poi presentato per 2 min, con gli altri partecipanti e gli investigatori che fungono da pubblico. Il discorso è stato interrotto a metà strada per le misurazioni., La sequenza delle procedure in questa fase è stata la seguente: (a) sedersi su una sedia disposta di fronte ad altri; (b) scegliere il tema del discorso; (c) pensare al tema per 1 min; (d) iniziare il discorso, che è stato interrotto dopo 1 min; (e) completare la scala di autovalutazione (fattori di ansia e sedazione VAMS) e misurazioni fisiologiche; (f) continuare il discorso per un altro minuto. Questa sequenza è durata per 5 min al massimo, in modo tale che, dopo 1 h, tutti i volontari avevano superato la procedura. La fase finale dello studio è iniziata 216 min dopo che il primo volontario aveva assunto il farmaco., Tutte le misurazioni sono state ripetute, mantenendo l’intervallo di 5 minuti per ogni volontario. La tabella 1 presenta uno schema della procedura sperimentale.

TABELLA 1. Calendario della sessione sperimentale.
Analisi statistica
Le caratteristiche cliniche e demografiche sono state analizzate con test non parametrici (genere) e analisi a un fattore della varianza (ANOVA; età, BMI e STAI-trait).,
I punteggi nei due fattori delle VAMS, pressione arteriosa sistolica e diastolica e frequenza cardiaca sono stati analizzati con un’analisi di varianza a misure ripetute (ANOVA a misure ripetute) inclusi i fattori “fase”, “gruppi” e interazione di gruppo di fase. Nei casi in cui le condizioni di sfericità non sono state raggiunte, i gradi di libertà del fattore ripetuto sono stati corretti con l’epsilon di Huynh-Feldt. I confronti tra i gruppi sono stati effettuati in ogni fase utilizzando un ANOVA a un fattore seguito da confronti multipli con il test Student-Newman-Keuls.,
L’analisi dei dati è stata eseguita utilizzando il pacchetto statistico per le scienze sociali (SPSS) versione 17 e il livello di significatività adottato è stato p < 0.05.
Risultati
Le caratteristiche demografiche e cliniche dei soggetti sono riportate nella Tabella 2. I gruppi non differivano significativamente per quanto riguarda i punteggi di genere, età, BMI e STAI-trait.

TABELLA 2. Caratteristiche demografiche e cliniche dei gruppi.,
Le misure ripetute ANOVA dei punteggi, nell’ansia fattore di VAMS ha mostrato un significativo effetto di fase (F3,162 = 60.24; p < 0.001), di gruppo (F4,54 = 3,25; p = 0,018) e fase-l’interazione di gruppo (F12,162 = 3.79; p < 0.001, Figura 1A). I confronti post hoc tra i gruppi in ogni fase hanno mostrato differenze significative (p < 0.05) tra PLAC e CLON nelle fasi di discorso e post-stress., I punteggi del gruppo CBD-300 erano significativamente diversi da quelli del gruppo CBD-900 nella fase di discorso e da quelli dei gruppi PLAC e CBD-100 durante la fase post-stress (p < 0.05). A titolo illustrativo, la figura 1B mostra la curva dose-risposta a forma di U invertita indotta dal CBD nella fase post-stress. Per quanto riguarda il fattore di sedazione delle VAMS, le misure ripetute ANOVA hanno mostrato effetti significativi della fase (F2.16,116.7 = 3.11; p = 0.028) e del gruppo (F4,54 = 3.48; p = 0.013, Figura 2A)., Un confronto generale post hoc tra i gruppi ha mostrato che il clonazepam ha indotto un effetto sedativo più elevato rispetto agli altri gruppi (effetto principale del trattamento). Un effetto simile è stato osservato nella fase post-stress (p < 0,05).
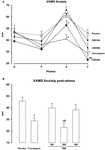
FIGURA 1. Cambiamenti nei punteggi del fattore di ansia della scala visiva analogica dell’umore (VAMS) (mm) indotta dal parlare in pubblico in volontari sani (A) durante al basale (B) e durante le fasi pre-stress (P), discorso (S) e post-stress (F) (A)., Per motivi di chiarezza, i risultati dell’ultima fase (F) sono anche mostrati come grafico a barre (B). I punti rappresentano i mezzi ± SEM di 11-12 soggetti. Gli asterischi ( ∗ ) indicano differenze statisticamente significative rispetto al gruppo placebo, (+) indica una differenza significativa rispetto al gruppo CBD-900 e (&) indica una differenza significativa rispetto al gruppo CBD-100.
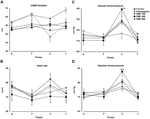
FIGURA 2., Cambiamenti nel fattore di sedazione della VAMS (mm, A), frequenza cardiaca , pressione arteriosa sistolica (C) e diastolica (D) (mm Hg) indotti dal parlare in pubblico in volontari sani. I punti rappresentano i mezzi ± SEM di 11-12 soggetti. Gli asterischi ( ∗ ) indicano differenze statisticamente significative rispetto agli altri gruppi, (&) indica una differenza significativa rispetto al clonazepam e ( $ ) indica una differenza significativa rispetto al gruppo CBD-100.,
Discussione
Abbiamo usato i TPSRS per indurre sperimentalmente l’ansia e abbiamo studiato se l’effetto ansiolitico del CBD negli esseri umani produce una curva dose-risposta a forma di U invertita. In linea prove precedenti (Zuardi et al., 2013), questo protocollo ha aumentato significativamente l’ansia soggettiva, la pressione sanguigna e la frequenza cardiaca, come dimostrato dall’effetto significativo della fase trovata in un’ANOVA ripetuta., Inoltre, il TPSRS era sensibile nel rilevare l’effetto ansiolitico del clonazepam, un noto farmaco ansiolitico, suggerendo che può essere utilizzato per identificare farmaci potenzialmente ansiolitici.
Alla dose di 300 mg, il CBD ha ridotto significativamente l’ansia soggettiva rispetto al gruppo PLAC durante la fase post-discorso del protocollo. Tuttavia, lo stesso non era vero per una dose inferiore (100 mg) o superiore (900 mg) del farmaco., Inoltre, anche i punteggi di ansia soggettiva del gruppo CBD-300 differivano significativamente da quelli del gruppo CBD-900 durante la fase del discorso e dal gruppo CBD-100 durante la fase post-discorso. Questi risultati suggeriscono che l’effetto ansiolitico acuto del CBD ha seguito una curva dose-risposta a forma di U invertita, che è coerente con i risultati degli studi sugli animali (Guimarães et al., 1990; Levin et al., 2014; Nazario et al., 2015; Peres et al., 2016). È interessante notare che la stessa dose di CBD che ha prodotto effetti ansiolitici (300 mg) non ha ridotto sistolica e DBP come clonazepam., Questa dissociazione tra effetti ansiolitici e simpaticoinibitori in seguito alla somministrazione acuta di CBD è coerente con le nostre osservazioni utilizzando l’SPST in volontari sani (Zuardi et al., 1993) e in pazienti con fobia sociale (Bergamaschi et al., 2011a).
Il meccanismo alla base di questo modello di effetto dose-risposta del CBD non può ancora essere completamente spiegato. Negli esseri umani, le aree cerebrali limbiche e paralimbiche sembrano essere coinvolte nell’azione ansiolitica del CBD., Ad esempio, studi con tomografia computerizzata a emissione di singolo fotone (SPECT) in volontari sani e pazienti naïve al farmaco con SAD hanno mostrato il coinvolgimento delle stesse aree implicate nell’effetto ansiolitico del CBD 400 mg, vale a dire il giro parahippocampale sinistro e il complesso amigdala-ippocampo sinistro (Crippa et al., 2004, 2011). Utilizzando la risonanza magnetica funzionale (fMRI) in volontari sani, i ricercatori hanno scoperto che il CBD 600 mg ha attenuato l’attivazione nell’amigdala e nella corteccia cingolata anteriore durante il riconoscimento di espressioni facciali spaventose (Fusar-Poli et al., 2009)., Gli autori hanno inoltre spiegato che questa azione del CBD è stata mediata da alterazioni nella connettività prefrontale sottocorticale tramite amigdala e corteccia cingolata anteriore (Fusar-Poli et al., 2010).
Nonostante l’identificazione di aree cerebrali che possono essere coinvolte nell’effetto ansiolitico del CBD, il meccanismo farmacologico specifico responsabile di questo effetto rimane da chiarire., CBD è un farmaco con molteplici obiettivi farmacologici, tra cui l’interazione con diversi recettori (CB1, CB2, GPR55, TRPV1, e 5-HT1A), interferenza con l’assorbimento e il metabolismo degli endocannabinoidi, e aumentare la neurogenesi ippocampale nel cervello adulto (Zuardi et al., 2017). Diversi studi hanno sostenuto il coinvolgimento dei recettori 5-HT1A nell’azione ansiolitica acuta del CBD., Ad esempio, l’effetto ansiolitico indotto da iniezioni periaqueductal gray (DPAG) sistemiche o intra-dorsali di CBD nei ratti è prevenuto da un antagonista del recettore 5-HT1A (Campos e Guimarães, 2008; Soares et al., 2010). Un’interazione simile tra i recettori CBD e 5-HT1A in altre strutture cerebrali legate al controllo di comportamenti ansiosi, come il nucleo del letto della stria terminallis o la corteccia frontale prelimbica, è anche coinvolta nell’attenuazione delle risposte all’ansia (Gomes et al., 2011, 2012; Fogaça et al., 2014)., Nelle cellule coltivate, il CBD è stato segnalato per agire come un agonista del recettore 5-HT1A (Russo et al., 2005), anche se studi recenti suggeriscono che questo non è il caso in fette o in condizioni vivo. La facilitazione della neurotrasmissione mediata da 5-HT1A da parte del CBD non sembra comportare il blocco della ricaptazione di 5-HT o cambiamenti nell’espressione di mRNA 5-HT1A nel DPAG dopo somministrazione cronica di CBD (Campos et al., 2013). Queste osservazioni suggeriscono che la modulazione dei recettori 5-HT1A da parte del CBD è complessa e potrebbe coinvolgere interazioni allosteriche (Rock et al., 2011).,
Come accennato in precedenza, i meccanismi responsabili della curva dose-risposta a forma di U invertita del CBD sono poco conosciuti. Potrebbero coinvolgere interazioni con il recettore vanilloide 1 o TRPV1. Ad alte concentrazioni, il CBD può attivare questi recettori e facilitare il rilascio di glutammato e le risposte difensive (Guimarães et al., 1991; Campos e Guimarães, 2009). Questo meccanismo potrebbe mascherare l’effetto ansiolitico del CBD mediato dai recettori 5-HT1A., Testare questa possibilità utilizzando iniezioni intra-DPAG in ratti, Campos e Guimarães (2009) ha dimostrato che il pretrattamento con un antagonista TRPV1 (capsazepina) ha trasformato una dose più alta e inefficace di CBD in un ansiolitico. Resta da testare se un meccanismo simile è coinvolto anche nella curva dose-risposta a forma di U osservata nel nostro studio. Consonante con precedenti prove che indicano che il CBD ha proprietà sedative più deboli rispetto alle benzodiazepine (Zuardi et al., 1993), la dose ansiolitica di CBD (300 mg) ha indotto un livello di sedazione significativamente più basso rispetto al clonazepam., È un vantaggio che deve essere evidenziato, poiché la sedazione e la compromissione della coordinazione motoria sono tra gli effetti avversi più comuni delle benzodiazepine, oltre alla potenziale dipendenza, ai deficit cognitivi e ai sintomi di astinenza, specialmente nella vecchiaia (Sgnaolin et al., 2016). Questi effetti collaterali non sono stati osservati con l’uso di CBD (Bergamaschi et al., 2011b).
I risultati riportati qui devono essere interpretati con cautela, dati i limiti del nostro studio., Innanzitutto, sarebbe stato auspicabile misurare i livelli plasmatici di CBD e clonazepam e mettere in relazione queste misurazioni con l’entità dei livelli di ansia; senza una curva dose-risposta, rimangono dubbi sul fatto che gli effetti del CBD seguano effettivamente una curva a forma di U invertita. Va notato, tuttavia, che precedenti indagini non sono state in grado di stabilire una relazione diretta tra i livelli plasmatici di CBD e i suoi effetti clinici (Agurell et al., 1986). Inoltre, la piccola dimensione del campione limita la potenza statistica dello studio., Inoltre, il design dello studio non ci consente di escludere la possibilità che un’altra dose moderata (ad esempio, 400 o 600 mg) possa aver avuto effetti ansiolitici ancora maggiori. Ad esempio, studi precedenti hanno dimostrato effetti ansiolitici acuti di 400 mg di CBD in studi SPECT su volontari sani (Crippa et al., 2004) e in pazienti con fobia sociale (Crippa et al., 2011) e di CBD 600 mg in un esperimento fMRI con uomini sani (Bhattacharyya et al., 2010)., Sebbene non sia necessario per questo studio proof of concept, queste limitazioni potrebbero essere superate in studi futuri che esaminano altre dosi 2-3 tra 300 e 900 mg per stabilire un vero indice terapeutico.
Conclusione
I nostri risultati sono in sintonia con le prove degli studi preclinici e supportano l’opinione che il CBD induca effetti ansiolitici acuti con una curva dose-risposta a forma di U invertita negli esseri umani. Questi risultati sottolineano l’importanza dell’attenta scelta degli intervalli di dose quando si studiano i potenziali effetti terapeutici del CBD., Ulteriori studi che valutano la curva dose-risposta del CBD in altre condizioni come la schizofrenia, il dolore, l’epilessia e il morbo di Parkinson e che coinvolgono la somministrazione cronica di CBD sono necessari per tradurre le evidenze precliniche nella pratica clinica e determinare la finestra terapeutica precisa del CBD per ogni condizione.
Contributi dell’autore
AZ, JH e JC hanno progettato lo studio. NR, AS e SB hanno condotto gli esperimenti. AZ e FG hanno condotto l’analisi statistica. AZ ha scritto la prima bozza del manoscritto., Tutti gli autori hanno contribuito e hanno approvato il manoscritto finale.
Dichiarazione di conflitto di interessi
AZ, JH, FG e JC sono co-inventori (Mechoulam R, JC, Guimaraes FS, AZ, JH, Breuer A) del brevetto “Fluorurati composti CBD, composizioni e loro usi. Pub. No.: WO / 2014 / 108899. Applicazione internazionale n.: PCT/IL2014”050023 ” Def. NOI no. Reg. 62193296; 29/07/2015; INPI il 19/08/2015 (BR1120150164927). L’Università di São Paulo ha concesso in licenza il brevetto a Phytecs Pharm (risoluzione USP n.15.1.130002.1.1)., L’Università di São Paulo ha un accordo con Prati-Donaduzzi (Toledo, Brasile) per ” sviluppare un prodotto farmaceutico contenente cannabidiolo sintetico e dimostrare la sua sicurezza ed efficacia terapeutica nel trattamento di epilessia, schizofrenia, morbo di Parkinson e disturbi d’ansia.”JH e JC hanno ricevuto supporto di viaggio da BSPG-Pharm.
Gli altri autori dichiarano che la ricerca è stata condotta in assenza di rapporti commerciali o finanziari che potrebbero essere interpretati come un potenziale conflitto di interessi.,
I revisori RWG, KA e handling Editor hanno dichiarato la loro affiliazione condivisa e l’Editor di handling afferma che il processo ha comunque soddisfatto gli standard di una revisione equa e obiettiva.
Riconoscimenti
AZ, JH, FG e JC sono destinatari del premio fellowship del Conselho Nacional de Desenvolvimento Científico e Tecnológico (CNPq, Brasile). Il presente studio è stato supportato da una sovvenzione CNPq (CNPq / MS/SCTIE / DECIT N∘ 26/2014 – Pesquisas sobre Distúrbios Neuropsiquiátricos; 466805/2014-4) e BSPG-Pharm (Sandwich, UK) ha gentilmente fornito CBD senza alcun costo.,
Campos, A. C., e Guimarães, F. S. (2008). Coinvolgimento dei recettori 5HT1A negli effetti ansiolitici del cannabidiolo iniettati nel grigio periaqueduttale dorsolaterale dei ratti. Psicofarmacologia (Berl) 199, 223-230. doi: 10.1007 / s00213-008-1168-per la prima volta, il progetto è stato pubblicato nel 2009, con il nome di”22d97200ec”(2009). Evidenza di un potenziale ruolo per i recettori TRPV1 nel grigio periaqueduttale dorsolaterale nell’attenuazione degli effetti ansiolitici dei cannabinoidi. Prog., Neuropsychopharmacol. Biol. Psychiatry 33, 1517–1521. doi: 10.1016/j.pnpbp.2009.08.017
PubMed Abstract | CrossRef Full Text | Google Scholar