Bevezetés
az alkének és alkinek olyan szénhidrogének, amelyek szén-szén kettős kötéssel, illetve szén-szén hármas kötésű funkcionális csoportokkal rendelkeznek. A molekuláris képletek ezek a telítetlen szénhidrogének tükrözik a többszörös kötés a funkcionális csoportok:
Alkének neve, ha voltak alkánok, de a “-ane” utótag megváltozott “-ene”., Ha az alkén csak egy kettős kötést tartalmaz, és a kettős kötés terminális (a kettős kötés a molekula egyik vagy másik végén van), akkor nem szükséges számot elhelyezni a név előtt.,
bután: C4H10 (CH3CH2CH2CH3)
buten: C4H8 (CH2=CHCH2CH3)
Ha a kettős kötést nem terminál (ha a szén-dioxid-valahol a közepén a lánc) akkor a szénatom kell ellátni oly módon, hogy az első két duplán ragasztott szénatom a legalacsonyabb szám, ez a szám kell előznie a “ene” utótagot kötőjellel, amint az alább látható.,
helyes: pent-2-ene (CH3CH=CHCH2CH3)
helytelen: pent-3-ene (CH3CH2CH=CHCH3)
a második helytelen, mivel a képlet vízszintes elfordítása alacsonyabb számot eredményez az alkén esetében.
Ha egy alkénben egynél több kettős kötés van, az összes kötést a molekula nevében kell számozni – még a terminális kettős kötéseket is. A számoknak a legalacsonyabbról a legmagasabbra kell menniük, vesszővel elválasztva egymástól. Az IUPAC numerikus előtagokat a kettős kötések számának jelzésére használják.,
octa-2,4-diene: CH3CH=CHCH=CHCH2CH2CH3
deca-1,5-diene: CH2=CHCH2CH2CH2CH3
molekula két kettős kötéssel elválasztva egyetlen kötés. Az ilyen állapotban lévő kettős kötéseket “konjugáltnak” nevezik, és a konformáció fokozott stabilitását képviselik, ezért energetikailag előnyben részesítik őket, mint reagensek sok helyzetben és kombinációban.,
| alkán | CnH2n+2 | ez egy adott számú szénatom maximális H/C aránya. |
|---|---|---|
| alkén | CnH2n | minden kettős kötés 2-vel csökkenti a hidrogénatomok számát. |
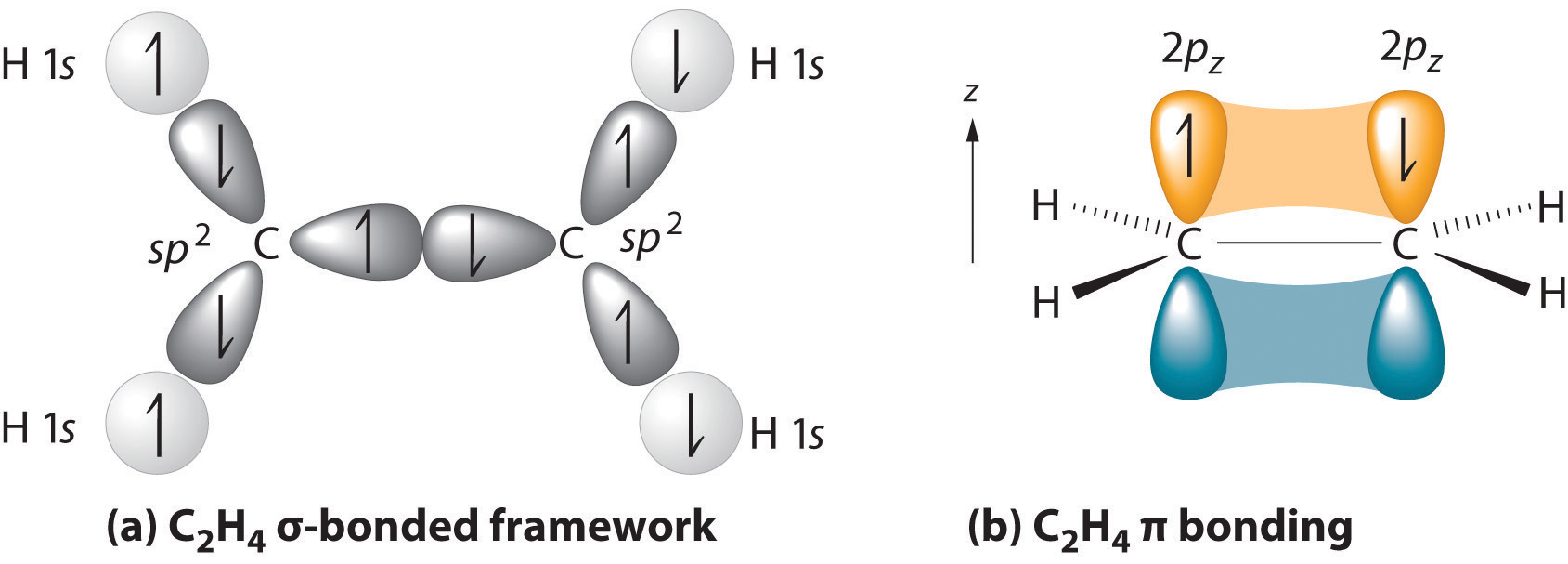
az alapszerkezet a leghosszabb lánc, amely a kettős kötés mindkét szénatomját tartalmazza., A két szénatommal a kettős kötés, valamint a négy atomok csatolt őket hazugság, a repülő, a bond szögek körülbelül 120° kettős kötés áll egy sigma kötelék alakult átfedés sp2 hibrid elektronpályák egy pi kötelék alakult átfedés párhuzamos 2 p elektronpályák
egy szénhidrogén molekuláris képlete információt nyújt az általa képviselt lehetséges szerkezeti típusokról. Vegyük például a c5h8 képlettel rendelkező vegyületeket., Az öt szén-alkán-pentán képlete C5H12, így a hidrogéntartalom különbsége 4. Ez a különbség arra utal, hogy az ilyen vegyületek hármas kötéssel, két kettős kötéssel, egy gyűrűvel plusz kettős kötéssel vagy két gyűrűvel rendelkezhetnek. Néhány példa itt látható, és legalább tizennégy másik van!