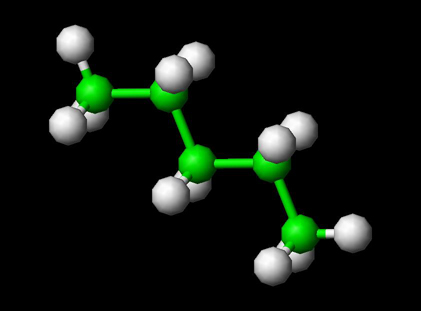
pour visualiser la molécule de Pentane en 3D —>>en 3D avec Jsmol
propriétés chimiques et physiques de la molécule de pentane
la conformation (forme) du pentane est linéaire, semblable à celle du butane, mais un atome de carbone plus long.
isomères
le Pentane est l’un des trois isomères structuraux de Formule moléculaire C5H12, les autres étant l’isopentane et le néopentane.,Les isomères ramifiés sont plus stables que le pentane, ce qui signifie qu’ils ont une chaleur de formation et une chaleur de combustion plus faibles. L’Isopentane est plus stable que le pentane de 1,8 kcal/mol et le néopentane de 5 kcal / mol. Un cycloalcane apparenté est le cyclopentane, bien que ce ne soit pas un isomère du pentane car sa formule moléculaire est différente, le cyclopentane est un isomère des pentènes.
utilisations
étant un hydrocarbure non fonctionnel, le pentane est un produit chimique de base. C’est principalement un carburant et un solvant, bien qu’il puisse également être utilisé comme source D’H2 via le reformage à la vapeur., En tant qu’hydrocarbure le plus volatil liquide à température ambiante, le pentane est souvent utilisé en laboratoire comme solvant pouvant être facilement évaporé. En outre, en raison de sa non-polarité et de son manque de fonctionnalité, son pouvoir de dissolution est faible, de sorte que seuls les composés non polaires ou riches en alkyles y sont solubles. Le Pentane est cependant complètement miscible avec de nombreux solvants courants tels que les chlorocarbures, les aromatiques, les éthers, mais pas les amines à chaîne courte ou les alcools à chaîne courte.,
réactions
le Pentane brûle pour former du dioxyde de carbone et de l’eau:
C5H12 + 8 O2- – – > 5 CO2 + 6 H2O
lorsque l’oxygène est limité, du carbone, du carbone partiellement oxydé (suie) et du monoxyde de carbone sont également formés.
comme pour les autres hydrocarbures, le pentane subit une chloration par radicaux libres:
C5H12 + Cl2- – – >C5H11Cl + HCl
de telles réactions sont non sélectives, donnant un mélange des 1-, 2-et 3-chloropentanes, ainsi que des dérivés plus fortement chlorés. D’autres halogénations radicalaires peuvent également se produire., Alors que le N-butane est la matière première conventionnelle de l’anhydride maléique de synthèse de duPont, le pentane est également un substrat:
CH3CH2CH2CH2CH3 + 5 O2 – – – >C2H2(CO)2O + 5 H2O + CO2
Voir aussi: