élimination sélective des composants
lors d’une expérience de synthèse d’un produit chimique, une réaction est souvent complète lorsque l’agitation ou le chauffage est cessé. Et pourtant, il y a toujours plus d’étapes dans la procédure! Ce qui arrive généralement directement après, c’est de « travailler » la réaction d’une manière ou d’une autre. Un work-up fait référence à des méthodes visant à isoler le produit du mélange réactionnel, et commence souvent par utiliser un entonnoir de séparation et des extractions.,

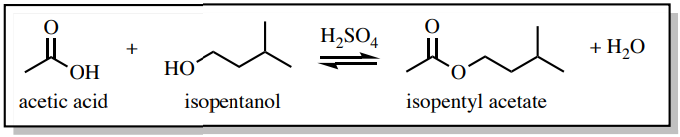
par exemple, imaginez que l’acide acétique et l’isopentanol aient été chauffés en présence d’un catalyseur acide pendant une heure (Figure 4.5) afin de fabriquer de l’acétate d’isopentyle, un ester qui sent la banane (voir Schéma de réaction à la Figure 4.6). Après la période d’une heure, il n’y a malheureusement pas seulement l’ester à l’odeur de banane dans le flacon., Le flacon contiendra également des sous-produits (l’eau dans ce cas), des restes de matériaux de départ si la réaction est incomplète, ainsi que les catalyseurs utilisés (\(\ce{H_2SO_4}\) dans ce cas). Dans cet exemple, il pourrait y avoir cinq composés dans le ballon de réaction après l’arrêt du chauffage (Figure 4.7)!
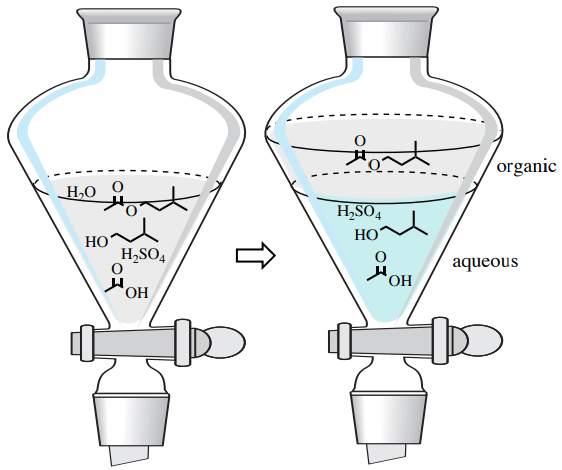
lors de la « préparation » de cette réaction, le mélange résultant est souvent versé dans un entonnoir de séparation avec de l’eau et du solvant organique. Cela produit deux couches dans l’entonnoir de séparation: une couche aqueuse et une couche organique.
après agitation de ce mélange hétérogène, les composés se distribuent en fonction de leur solubilité. Les composés qui ont une solubilité élevée dans l’eau favorisent la couche aqueuse tandis que les composés moins polaires favorisent la couche organique., Dans cet exemple, le catalyseur acide et l’acide carboxylique résiduel ou l’alcool seraient probablement aspirés dans la couche d’eau. L’ester aurait une plus grande affinité pour la couche organique que la couche aqueuse, ce qui l’isolerait des autres composants du mélange réactionnel (Figure 4.7).
dans cet exemple, il est possible que de petites quantités d’alcool soient également aspirées dans la couche organique, mais elles pourraient probablement être éliminées avec un lavage à l’eau. »Dans un lavage, le composé désiré (par exemple l’acétate d’isopentyle), reste dans sa couche actuelle de l’entonnoir de séparation (dans cet exemple la couche organique), et les composés indésirables sont éliminés, ou « emportés » dans une autre couche (par exemple la couche aqueuse). Un lavage est différent d’une extraction, car dans une extraction, le composé désiré se déplace de son emplacement actuel (c.-à-d., se déplace d’une couche aqueuse à une couche organique), tandis que dans le lavage, le composé souhaité reste dans sa couche actuelle.