hasta ahora, hemos analizado las formas en que los pares de orbitales atómicos podrían combinarse para formar orbitales moleculares to para formar enlaces. Así como pensamos que hay una progresión de orbitales atómicos de la energía más baja a la más alta (1s, 2s, 2p, 3s…), podemos organizar estos orbitales moleculares por orden de su energía.
en gran medida, se puede considerar que el orden de los orbitales moleculares en energía sigue el orden de los orbitales atómicos a partir de los cuales están construidos., Hay algunas desviaciones de esa regla, a veces, pero ese es el lugar más simple para comenzar. Así, en una molécula, los orbitales moleculares de menor energía serían los formados a partir de los orbitales atómicos de menor energía, los orbitales 1s.
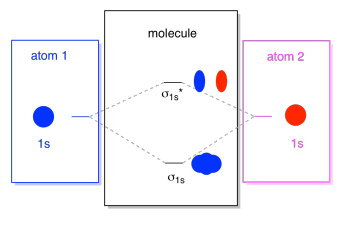
lo que vemos aquí es un diagrama de interacción orbital molecular. El centro del diagrama es sólo el diagrama de energía orbital molecular. Es análogo al diagrama de energía Orbital atómica (que va 1s, 2s, 2p, 3s…). El orden de la energía hasta ahora es σ1s, σ1s*., Los lados del diagrama simplemente se refieren a dónde vinieron esos orbitales moleculares, con líneas punteadas para guiarlo de un lugar a otro. En conjunto, la imagen dice que el orbital 1s en un átomo y el orbital 1s en el otro átomo pueden combinarse de dos maneras diferentes, produciendo la σ1s de menor energía y la σ1s de mayor energía y anti-enlace*.
tenga en cuenta que aún no hemos agregado ningún electrón a ese diagrama de energía orbital molecular, pero cuando lo hagamos, simplemente los rellenaremos de abajo hacia arriba, Al igual que lo haríamos con un diagrama de energía Orbital atómica.,
el siguiente conjunto más bajo de orbitales atómicos es el nivel 2s. Estos orbitales esféricos se combinarían muy parecido a los orbitales 1s, y obtendríamos un diagrama similar, solo que a un nivel de energía ligeramente superior.
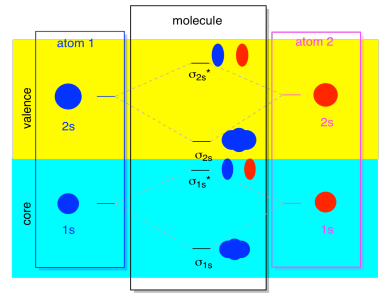
La mayoría de las veces, no vamos a ver tanto las σ1s como las σ2s mostradas en el diagrama. Eso es porque si hay electrones 2s, entonces esos electrones 1s son realmente electrones centrales, no Valencia. Están enterrados un poco más profundamente en el átomo, y no juegan un papel muy importante en la Unión., Ignorar los electrones del núcleo es bastante común; si recuerdan, en configuraciones de electrones atómicos podríamos escribir 2s22p4 en lugar de 1s22s22p4 para oxígeno; estábamos ignorando el núcleo. Cuando dibujamos las estructuras de Lewis, le dimos al oxígeno seis electrones, en lugar de ocho; estábamos ignorando el núcleo.
en el contexto de MO, supongamos que tenemos electrones 2s. Eso debe significar que cada átomo tiene dos electrones 1s propios, para un total de cuatro. Cuando esos cuatro electrones se llenan en el diagrama de MO de abajo hacia arriba, ocuparán tanto los σ1s de Enlace como los σ1s anti-enlace*., El efecto de ambas combinaciones ocupadas es cancelar el enlace; esos dos pares de electrones permanecen sin enlace. Así que podemos ignorarlos y realmente no nos estamos perdiendo nada.
los orbitales 2s no son los únicos en el segundo shell. También hay orbitales 2p. Recuerde, hay un par de formas muy diferentes en las que los orbitales p pueden combinarse entre sí, dependiendo de qué eje se encuentran. Si no se encuentran paralelos entre sí, es decir, si son perpendiculares entre sí, como un px y un py, entonces no pueden interactuar entre sí en absoluto., El pz en un átomo podría interactuar con el Pz en el otro átomo, sin embargo, porque son paralelos entre sí.
Por lo general, definimos el eje z como que se encuentra a lo largo de la línea entre los dos átomos que estamos mirando. Dos orbitales pz se encuentran a lo largo de ese eje, cada uno con un lóbulo que se extiende en el espacio entre los átomos, y cada uno con otro lóbulo que se extiende, en la otra dirección
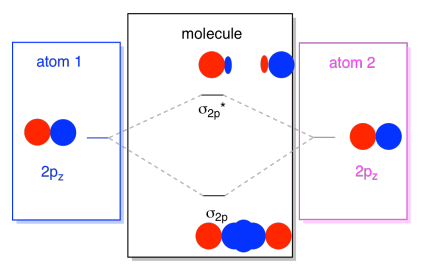
Las combinaciones resultantes se llaman σ porque se encuentran a lo largo del eje entre los átomos (eso es exactamente lo que σ significa, en términos de enlace)., Hay una combinación σ, Si los lóbulos superpuestos están en fase entre sí, y una combinación σ*, si esos lóbulos están fuera de fase entre sí. Debido a que estos nuevos orbitales surgen de los orbitales atómicos 2p, los llamamos σ2p y σ2p*.
también hay aquellos orbitales p que no se encuentran a lo largo del eje de enlace, o el eje entre los dos átomos. Los orbitales px son perpendiculares a los orbitales pz que acabamos de ver, y por lo tanto perpendiculares al eje entre los enlaces. Sin embargo, todavía son paralelas entre sí, y todavía pueden formar combinaciones., Estos dos orbitales formarían una combinación en fase y una combinación fuera de fase.
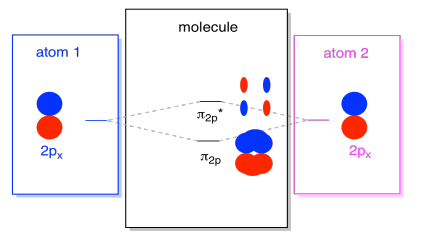
tenga en cuenta que la separación energética entre estas dos combinaciones es un poco más pequeña que la brecha entre los niveles σ2p y σ2p*. La diferencia está relacionada con el grado de superposición entre los orbitales atómicos. Los orbitales en el eje se proyectan fuertemente en el mismo espacio; se superponen mucho e interactúan fuertemente. Los orbitales fuera del eje se rozan unos contra otros, interactuando con menos fuerza y dando como resultado cambios energéticos más pequeños., La brecha entre el orbital n2p y el orbital N2P* es por lo tanto mucho más pequeña que la que existe entre los orbitales σ2p y σ2p*.
en realidad hay dos de esos orbitales p fuera del eje. Además del conjunto px, tendríamos un conjunto py. Si el conjunto px está en el plano de la pantalla, el conjunto py tiene un orbital que sobresale por delante y otro oculto detrás. Sin embargo, las combinaciones entre los dos orbitales py son exactamente las mismas que vimos entre los dos orbitales px. Simplemente se giran en un plano perpendicular con respecto a las combinaciones px.,
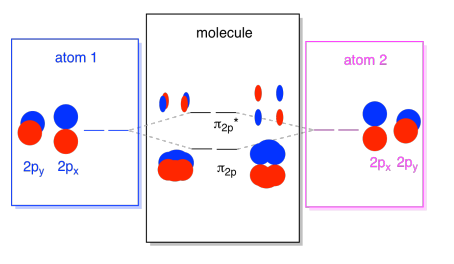
podemos poner todos esos orbitales basados en 2p juntos en un diagrama. Está empezando a llenarse un poco más, pero este diagrama es solo una combinación de las piezas que ya hemos visto. Tenga en cuenta que los orbitales atómicos px, py y pz comienzan con la misma energía (los hemos apilado aquí para que pueda ver la correlación entre los orbitales atómicos y moleculares). Esto significa que los orbitales N2P & N2P* estarán «anidados» entre los orbitales σ2p & σ2p*.,
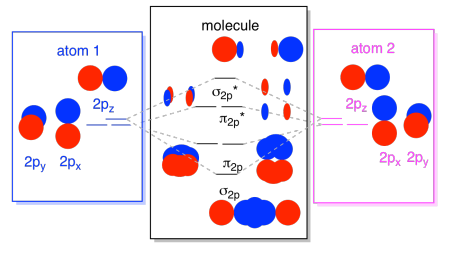
finalmente, teniendo en cuenta que los orbitales 2p son más altos en energía que los orbitales 2s, podemos combinar esas imágenes en un diagrama. Una vez más, hemos visto estas piezas individuales antes; solo las estamos ensamblando ahora.
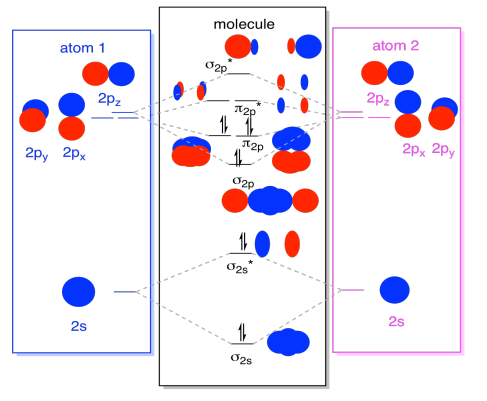
Mientras estamos en ello, nos pueden agregar en los electrones. ¿Cómo? Es sólo el número total de electrones de Valencia. Por ejemplo, hemos utilizado N2., Cada nitrógeno tiene cinco electrones de Valencia, para un total de diez, así que acabamos de llenar diez electrones, comenzando en la parte inferior del diagrama de nivel de energía orbital molecular. Si esta fuera otra molécula, como F2 u O2, construiríamos el diagrama general de una manera similar, pero solo usaríamos un número diferente de electrones.
la imagen orbital que hemos descrito anteriormente es realmente solo una imagen potencial de la estructura electrónica del dinitrógeno (y cualquier otro grupo principal o diatómico de bloque p)., No obtendremos una imagen real de la estructura del dinitrógeno hasta que poblemos estos niveles potenciales con electrones.
- solo los niveles de energía con electrones tienen un efecto sobre la energía (y el comportamiento) de la molécula.
En otras palabras, la energía de los electrones determina el comportamiento de la molécula. Los otros niveles de energía son solo posibilidades que permanecen insatisfechas.
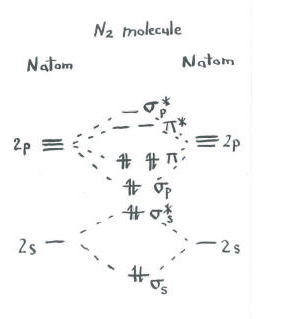
Pensar acerca de la imagen de dinitrógeno.
- Cada nitrógeno tiene cinco electrones de Valencia.
- Hay un total de diez electrones.,
- Dos entran cada uno en los niveles s S bonding y s s* antibonding. Recuerde, los mantuvimos separados del conjunto de p como una simplificación.
- Dos entran cada uno en la Unión s p y cada uno de los niveles de unión P.
los orbitales restantes (s p* antibonding y cada uno de los niveles p * antibonding) están desocupados. Estos son niveles imaginarios que no juegan un papel en la determinación de la energía del dinitrógeno. En un cálculo orbital molecular real, los electrones en estos niveles contribuirían a la energía total de la molécula.,
obtenemos información adicional de esta imagen. Por ejemplo, podemos ver el orden del enlace en dinitrogen.
- El orden de enlace es solo el número de enlaces entre un par de átomos.
- El bono es uno de varios factores que influye en la fuerza del enlace covalente.
- cuanto mayor sea el orden de enlace, más electrones se comparten entre los átomos, y más fuerte es el enlace.
en dinitrogen, los niveles de unión s S S * antibonding se cancelan entre sí. Un par es más bajo en energía que en el átomo, pero el otro es más alto., No hay reducción neta de energía. Estos electrones no contribuyen a un enlace nitrógeno-nitrógeno. Estos son pares de electrones no enlazantes.
los seis electrones en el enlace s p y los niveles de enlace p, sin embargo, representan una disminución en la energía de los niveles de energía en los átomos de nitrógeno libres. Estos tres pares de electrones de baja energía indican tres enlaces entre los átomos de nitrógeno.
recuerde, hemos hecho algunos atajos en esta imagen, y un cálculo orbital molecular real podría dar resultados ligeramente diferentes., Sin embargo, todavía revelaría un orden de enlace de tres, así como dos pares de electrones no enlazantes.
además, a veces las imágenes orbitales moleculares se muestran de diferentes maneras. Un diagrama de interacción orbital molecular muestra cómo los orbitales atómicos o moleculares se combinan para formar nuevos orbitales. A veces, podemos estar interesados solo en los niveles de energía orbitales moleculares en sí mismos, y no de dónde vinieron. Un diagrama de nivel de energía orbital molecular solo muestra los niveles de energía en la molécula., Con frecuencia, pero no siempre, los diagramas de nivel de energía se muestran sin ninguna imagen de los orbitales, con el fin de centrar la atención en los niveles de energía, que de una manera fundamental son la parte más importante de la imagen. Además, debido a que solo los niveles de energía ocupados realmente contribuyen a la energía de la molécula, a veces los orbitales desocupados de mayor energía quedan fuera de la imagen.

muy a menudo los resultados de los cálculos de orbitales moleculares refuerzan lo que podríamos predecir de las estructuras de Lewis., Si dibujas una estructura de Lewis de dinitrógeno, también predecirás un triple enlace nitrógeno-nitrógeno. La principal ventaja de la teoría de orbitales moleculares es que permite la predicción cuantitativa de la energía cuando hacemos un cálculo real en una computadora. Además, es importante darse cuenta de que no hay una razón real para la regla del octeto a menos que consideremos la mecánica cuántica. Las estructuras de Lewis se basan en una observación empírica de que los electrones forman pares y octetos, sin intentar explicar por qué., La teoría de orbitales moleculares toma algunas relaciones fundamentales de la física y las aplica a moléculas muy complicadas con muy buen éxito. Con solo conocer el número de electrones en la molécula, y saber aproximadamente dónde se encuentran los núcleos en la estructura, los cálculos de orbitales moleculares proporcionan información muy útil sobre la energía. Además, en casos más complicados que N2, estos cálculos pueden incluso corregir nuestra primera suposición sobre la geometría molecular y dónde se encuentran los enlaces.,
ejercicio \(\PageIndex{2}\)
Un diagrama orbital Molecular para una molécula diatómica (dos átomos) varía en el número de electrones. ¿Cómo poblas los electrones?
Answer
* cuenta los electrones de Valencia en la molécula. Es el número de electrones de Valencia en cada átomo, ajustado para cualquier carga en la molécula. (por ejemplo, C22-tiene 10 electrones de Valencia: 4 de cada carbono that eso es 8 and y dos más para la carga 2).
• Fill electrons into the lowest energy orbitales first.
• pares de electrones después de que todos los orbitales en el mismo nivel de energía tienen un electrón.,
ejercicio \(\PageIndex{3}\)
construir un diagrama orbital molecular cualitativo para el cloro, Cl2. Compare el orden de enlace con el visto en la estructura de Lewis (recuerde que un electrón en un orbital antibonding cancela la estabilización debido a la Unión de un electrón en un orbital bonding).
Answer 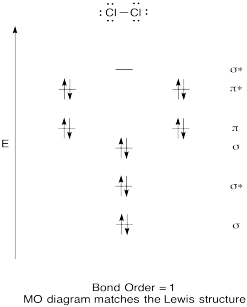
Exercise \(\PageIndex{4}\)
- construir un diagrama orbital molecular cualitativo para oxígeno, O2.
- Compare el orden de enlace con el visto en la estructura de Lewis.,
- ¿De qué otra manera se compara esta imagen de MO del oxígeno con la estructura de Lewis? ¿Qué te dicen las dos estructuras sobre el emparejamiento de electrones?
- Los compuestos que tienen todos sus electrones emparejados se conocen como diamagnéticos. Aquellos con electrones no emparejados se conocen como paramagnéticos. Los materiales paramagnéticos son atraídos por un campo magnético, pero las cosas diamagnéticas no lo son. ¿Cómo esperarías que se comportara el oxígeno molecular?,
Answer
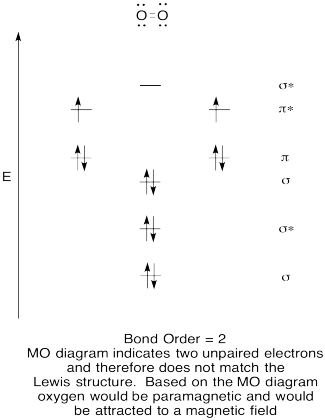
Exercise \(\PageIndex{5}\)
- construir un diagrama orbital molecular cualitativo para el anión peróxido, O22-.
- Compare el orden de enlace con el visto en la estructura de Lewis.
- ¿De qué otra manera se compara esta imagen de MO del oxígeno con la estructura de Lewis? ¿Qué te dicen las dos estructuras sobre el emparejamiento de electrones?,
- basado en imágenes orbitales moleculares, ¿con qué facilidad cree que el dioxigeno podría reducirse a peróxido (mediante la adición de dos electrones)?
Answer
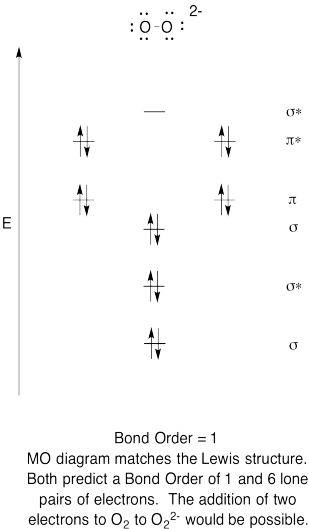
Exercise \(\PageIndex{6}\)
construir un diagrama orbital molecular cualitativo para diboron, B2. ¿Cree que los enlaces Boro-Boro podrían formarse fácilmente, basándose en esta imagen?,
Answer
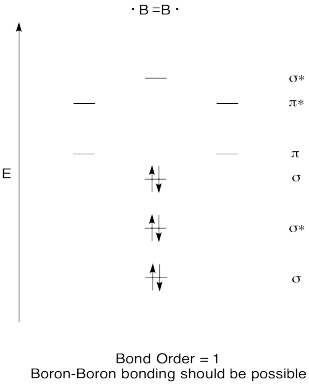
Exercise \(\PageIndex{7}\)
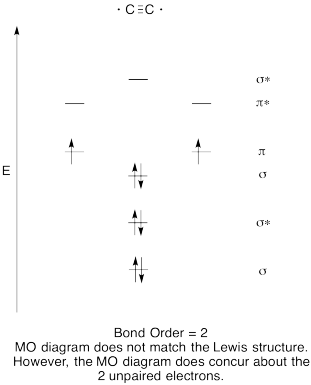
- construir un diagrama orbital molecular cualitativo para dicarbono, C2.
- Compare el orden de enlace con el visto en la estructura de Lewis.
- ¿De qué otra manera se compara esta imagen de MO del oxígeno con la estructura de Lewis? ¿Qué te dicen las dos estructuras sobre el emparejamiento de electrones?,
Answer
Exercise \(\PageIndex{8}\)
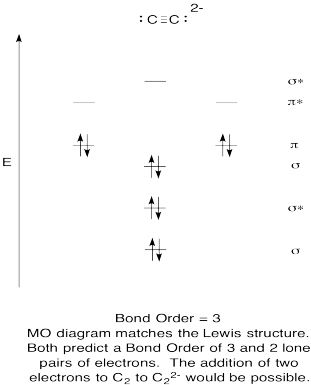
- construir un diagrama orbital molecular cualitativo para el anión acetiluro, C22-.
- Compare el orden de enlace con el visto en la estructura de Lewis.
- ¿De qué otra manera se compara esta imagen de MO del oxígeno con la estructura de Lewis? ¿Qué te dicen las dos estructuras sobre el emparejamiento de electrones?,
- basado en imágenes orbitales moleculares, ¿con qué facilidad cree que el dicarbono podría reducirse a acetiluro (mediante la adición de dos electrones)?
Answer
Exercise \ (\PageIndex{9}\)
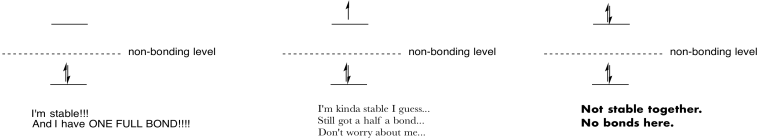
Haga dibujos y notas para resumir el efecto de rellenar orbitales antibonding.
Respuesta
Atribución
Chris P Schaller, D. Tel.,, (College of Saint Benedict / Saint John’s University)