introduktion
koncentration er målet for, hvor meget af et givet stof der blandes med et andet stof. Opløsninger siges at være enten fortyndet eller koncentreret. Når vi siger, at eddike er \(5\%\) eddikesyre i vand, giver vi koncentrationen. Hvis vi sagde, at blandingen var \(10\%\) eddikesyre, ville dette være mere koncentreret end eddikeopløsningen.,
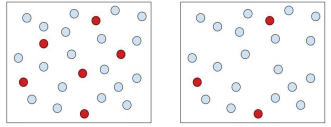
en koncentreret opløsning er en, hvor der er en stor mængde opløst stof i en given mængde opløsningsmiddel., En fortyndet opløsning er en, hvor der er en lille mængde opløst stof i en given mængde opløsningsmiddel. En fortyndet opløsning er en koncentreret opløsning, der i det væsentlige er blevet vandet. Tænk på de frosne juicebeholdere, du køber i købmanden. For at fremstille juice skal du blande det frosne juicekoncentrat inde fra disse containere med tre eller fire gange beholderens størrelse fuld af vand. Derfor fortynder du den koncentrerede juice. Med hensyn til opløst stof og opløsningsmiddel har den koncentrerede opløsning en masse opløst stof i forhold til den fortyndede opløsning, der ville have en mindre mængde opløst stof.,
udtrykkene “koncentreret” og “fortyndet” tilvejebringer kvalitative metoder til at beskrive koncentration. Selvom kvalitative observationer er nødvendige og har deres plads i alle dele af videnskaben, inklusive Kemi, vi har set gennem vores undersøgelse af videnskab, at der er et klart behov for kvantitative målinger i videnskaben. Dette gælder især i opløsningskemi. I dette afsnit vil vi undersøge nogle kvantitative metoder til at udtrykke opløsningskoncentration.