Kategorie: chemie
Publikováno: prosinec 9, 2013
Ano, voda může zůstat tekutá pod nulovými stupni Celsia. Existuje několik způsobů, jak se to může stát.
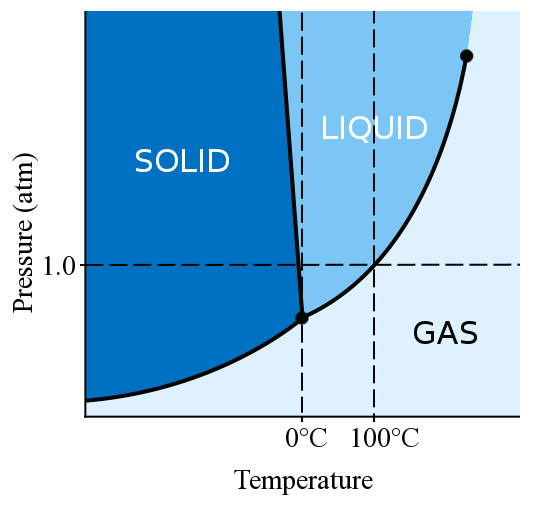
nejprve závisí fáze materiálu (ať už je to plyn, kapalina nebo pevná látka) silně na jeho teplotě i tlaku., U většiny kapalin zvyšuje tlak teplotu, při které kapalina zmrzne na pevnou látku. Pevná látka se vytvoří, když se volné, meandrující molekuly kapaliny dostanou dostatečně pomalu a dostatečně blízko, aby vytvořily stabilní vazby, které je připínají na místo. Když aplikujeme tlak na kapalinu, donutíme molekuly, aby se přiblížily k sobě. Mohou proto vytvářet stabilní vazby a stát se pevnými, i když mají při standardním tlaku vyšší teplotu než bod mrazu. Voda je ale poněkud unikátní. Molekuly vody se šíří, když se spojují do pevné krystalické struktury., Tato rozšiřující se akce vede k tomu, že led je méně hustý než kapalná voda, což způsobuje, že se led vznáší. Toto šíření-out působení molekul vody během zmrazení také znamená, že použití tlaku na vodu snižuje bod mrazu. Pokud použijete dostatečný tlak (což ztěžuje rozložení molekul vody do pevné struktury), můžete mít tekutou vodu několik stupňů pod nulou stupňů Celsia.
i když neaplikujete tlak, stále můžete mít kapalnou vodu při teplotách pod nulou pomocí přísad., Přísady, jako je sůl, mohou interferovat s chemickým spojením potřebným k vytvoření pevné látky, a proto mohou snížit bod tuhnutí vody. Sůl se skládá ze silných iontů sodíku a chloru. Když se rozpustí ve vodě, molekuly vody mají tendenci se držet solných iontů místo k sobě navzájem, a proto nemrznou tak snadno. Jak přidáte více soli do vody, jeho bod tuhnutí stále klesá, dokud voda nedosáhne nasycení a nemůže držet žádnou další sůl. Pokud přidáte dostatek soli, bod mrazu vody může klesnout až na -21 stupňů Celsia., Tato skutečnost znamená, že voda při -21 stupních Celsia může zůstat tekutá, pokud se přidá dostatek soli. Namísto udržování tekuté vody před mrazem lze tuto silnou vlastnost soli použít také k přeměně ledu zpět na vodu. Kropení soli na ledových chodnících snižuje bod mrazu ledu pod okolní teplotu a LED se taví. Kropení soli na ledových chodnících však nepomůže, pokud je okolní teplota pod -21 stupňů Celsia. Vliv soli na bod mrazu vody má také hluboké účinky na oceány Země.,
i když neaplikujete tlak a do vody nic nepřidáte, stále můžete mít kapalnou vodu při teplotách pod nulou stupňů Celsia. Aby voda zamrzla na led, potřebuje něco, na co by se mělo zmrazit, aby se proces zahájil. Tyto výchozí body nazýváme „nukleační centra“. Ve většině situací trochu prachu, nečistot nebo dokonce malých vibrací ve vodě poskytuje nukleační Centra pro zmrazení vody. Ale pokud je vaše voda velmi čistá a velmi klidná, není nic, na co by molekuly vody krystalizovaly., V důsledku toho můžete ochladit velmi čistou vodu hluboko pod nulou stupňů Celsia bez zmrazení. Voda v tomto stavu se nazývá „podchlazená“. Při standardním tlaku může být čistá voda podchlazena až na -40 stupňů Celsia. Podchlazená voda je chráněna před mrazem pouze nedostatkem nukleačních Center. Proto, jakmile jsou k dispozici nukleační centra (což by mohlo být stejně jednoduché jako vibrace), podchlazená voda rychle zamrzne. Mrznoucí déšť je přirozeným příkladem podchlazené kapalné vody., Jakmile mrznoucí déšť zasáhne objekt na zemském povrchu, tento objekt poskytuje nukleační centra a déšť zamrzne na led.
témata: zmrazení, bod mrazu, mrznoucí déšť, led, fázový diagram, tlak, podchlazení, teplota, voda