Úvod
několik studií na zvířatech však ukázalo, že CBD produkuje obrácené křivky dávkové odpovědi ve tvaru písmene U. Tyto křivky byly poprvé popsány u potkanů testovaných v modelu úzkosti zvýšené Plus maze (EPM) (Guimarães et al., 1990). V této studii CBD zvýšil průzkum otevřených paží (anxiolytický účinek) v dávkách 2, 5-10 mg/kg, ale ne 20 mg/Kg (Guimarães et al., 1990)., Podobné křivky dávkové odpovědi ve tvaru zvonu byly popsány v jiných studiích zkoumajících behaviorální účinky CBD. Například, danio pruhované léčených 0,5 mg/kg CBD strávil podstatně více času v horní zóně akvária (což je interpretováno jako anxiolytikum-jako účinek), zatímco chování ryb ošetřených nejnižší (0,1 mg/kg) a nejvyšší dávky (5 a 10 mg/kg) se nelišila od kontrol (Nazario et al., 2015). Podobný vzorec byl také pozorován u spontánně hypertenzních potkanů (SHRs), které představují fenotyp podobný schizofrenii., Inhibice prepulse u tohoto kmene potkanů byla obrácena o 30 mg / kg CBD, ale ne o dávky 15 a 60 mg/kg (Levin et al., 2014). Totéž bylo pozorováno pomocí modelu kognitivních poruch indukovaných reserpinem u potkanů, zvířecího modelu Parkinsonovy choroby i tardivní dyskineze. Zatímco CBD v dávce 0, 5 mg/kg oslabil deficit paměti vyvolaný reserpinem v diskriminačním úkolu, dávka 5 mg/kg se ukázala jako neúčinná (Peres et al., 2016).,
existuje jasná potřeba prozkoumat nové způsoby zvládání úzkostných poruch, protože jejich léčba zůstává problematická a obvykle zahrnuje kombinaci léků, včetně benzodiazepinů a antidepresiv. Tyto léky mají své nevýhody, jako je riziko závislosti a abstinenční syndrom, sexuální vedlejší účinky, kognitivní a psychomotorické postižení, opožděný nástup účinku (antidepresiva), nízké přijetí, a požadavek na pečlivé dávkování ovládání (Katzman et al., 2014; Bandelow et al., 2015; Sgnaolin et al., 2016)., Zdá se, že CBD nevyvolává významné nežádoucí účinky u lidí (Bergamaschi et al., 2011b). Z možného terapeutického hlediska je však nezbytné určit, zda je podobný obrácený vzorec dávkové odpovědi ve tvaru písmene U přítomen také u lidí. Abychom tuto možnost prozkoumali, vybrali jsme jeden z nejkonzistentnějších účinků CBD, akutní pokles úzkosti. Tento účinek byl popsán u několika zvířecích modelů a u zdravých dobrovolníků a pacientů se sociální úzkostnou poruchou (SAD) (Guimarães et al., 1990; Zuardi et al., 1993; Bergamaschi et al., 2011A; Crippa et al.,, 2011); nebyla však zkoumána pomocí více dávek u lidí.
jednou široce používanou metodou pro vyvolání experimentální úzkosti u lidí je simulovaná řečnická úloha (SPST-Graeff et al., 2003). SPST je velmi konzistentní při zvyšování sebehodnocení úzkosti. Jeho účinky na fyziologické reakce (srdeční frekvence, krevní tlak a sekrece kortizolu) jsou však méně konzistentní (Palma et al., 1994; Hetem et al., 1996; de-Paris et al., 2003)., Meta-analýza 11 studií, které používají SPST to potvrdil pozorování, ukazující výrazný nárůst celkové velikosti účinku na subjektivní úzkost, ale ne na systolický krevní tlak (SBP) a srdeční frekvence (Zuardi et al., 2013). Řídké důkazy v literatuře naznačují, že veřejné mluvení v situaci v reálném životě je účinnější pro zvýšení fyziologických odpovědí (Turner et al., 1990; Dickerson and Kemeny, 2004). V nedávné studii jsme porovnali test veřejného mluvení v reálné situaci (TPSRS) a SPST., Výsledky ukázaly, že obě metody jsou účinné při zvyšování subjektivní úzkost, ale pouze TPSRS zvýšená srdeční frekvence, SBP, a diastolický krevní tlak (DBP) (Zuardi et al., 2013).
tato studie byla proto navržena tak, aby otestovala hypotézu, že zvýšení dávek CBD by vyvolalo anxiolytické účinky v obráceném vzoru dávkové odpovědi ve tvaru písmene U U zdravých dobrovolníků předložených TPSRS.,
Materiály a Metody
Témata
Šedesát zdravých mužů a žen ve věku 18-35 let, bez historie minulosti nebo současné psychiatrické onemocnění, alkohol nebo jiné drogové závislosti byly přijímáni prostřednictvím inzerátu v kampusu University of São Paulo v Ribeirão Preto. Účastníci s velkými zdravotními stavy nebo kteří užívali léky s potenciálem zasahovat do výsledků studie nebyli zahrnuti., Dobrovolníci byli dotazováni za účelem posouzení způsobilosti a měřit jejich sklon k úzkosti přes vlastnost verze Spielbergerem State-Trait Anxiety Inventory (STAI – Spielbergerem et al., 1970). Způsobilí účastníci, kteří souhlasili s účastí byli instruováni, aby se zdržely drogy v týdnu před konáním zkoušky a z alkoholu a kofeinu 24 hodin před zkouškou., Všichni dobrovolníci podepsali písemný informovaný souhlas k účasti poté, co byl plně informován o výzkumných postupů, které byly v souladu se stávající podmínky, Helsinské Deklarace a byly schváleny Etickou komisí Ribeirão Preto Lékařské fakultě Univerzitní Nemocnice (HCRP -Č. 12407/09).
dobrovolníci byli náhodně přiděleno do pěti skupin s 12 předměty každý dostávat různé dávky CBD (100, 300 a 900 mg), clonazepam (1 mg) nebo placebem v dvojitě zaslepené, randomizované designu., Skupiny byly porovnány podle pohlaví, věku, indexu tělesné hmotnosti (BMI) a skóre STAI-trait. Jeden dobrovolník ze skupiny CBD – 300 se nemohl zúčastnit experimentálního zasedání kvůli osobním problémům a byl stažen ze studie.
léky
Kanabidiolový prášek s čistotou 99, 6% (bez přítomnosti jiných kanabinoidů) rozpuštěný v kukuřičném oleji v dávkách 100 a 200 mg/ml byl laskavě poskytnut Biosynthesis Pharma Group (BSPG-Pharm, Sandwich, UK). Roztok CBD, tablety clonazepamu (Rivotril®, Roche Lab) a placebo (kukuřičný olej) byly baleny ve stejných želatinových kapslích., Všichni dobrovolníci obdrželi pět tobolek jeden mililitr každý, v následujících kombinacích: pět kapsle obsahující kukuřičný olej (placebo skupina); jedna tobolka CBD 100 mg/ml a čtyři tobolky kukuřičný olej (CBD-100 skupina); tři kapsle CBD 100 mg/ml a dvě tobolky kukuřičný olej (CBD-300 skupina); čtyři kapsle CBD 200 mg/ml a jedna tobolka CBD 100 mg/ml (CBD-900 group); a jedna tobolka s clonazepam a čtyři tobolky kukuřičný olej (clonazepam skupiny – CLON)., Každé ošetření dostalo náhodné číslo a jak vyšetřovatel odpovědný za dávkování kapslí, tak dobrovolník nevěděli o jejich obsahu (dvojitě zaslepený). Nakonec byla volba intervalu mezi podáním léčiva a tpsrs založena na předchozích farmakologických studiích, které ukázaly, že maximální plazmatické koncentrace CBD a klonu užívané perorálně se obvykle vyskytují mezi 2 a 3 hodinami po požití (Agurell et al., 1981; Crevoisier et al., 2003; Borgwardt et al., 2008; Fusar-Poli et al., 2009; Martin-Santos et al., 2012)., CBD prochází významným účinkem prvního průchodu, což vede k tvorbě řady metabolitů a bylo zjištěno, že jeho poločas u lidí je mezi 2 a 5 dny po perorálním podání. Biologická dostupnost orálního CBD u lidí je kolem 6%, což podporuje názor, že má významný efekt prvního průchodu (Zhornitsky a Potvin, 2012). Průměrná plazmatická hladina CBD při 1, 2 a 3 h po akutním podání 600 mg byla 0, 36, 1, 62 a 3, 4 ng/ml (Martin-Santos et al., 2012)., Výběr dávek použitých v této studii byl založen na předchozích důkazech, které ukazují, že akutní Perorální podání 300 mg CBD mělo anxiolytické účinky v SPST (Zuardi et al., 1993).
Psychologické Měření
Dva faktory Vizuální Analogové Náladu Měřítku (VAMS), přeložen a ověřen do portugalštiny Zuardi a Karniol (1981), byly použity pro vyhodnocení úrovně úzkosti a uklidňující účinky v průběhu zkoušky. Vas je samoobslužný nástroj sestávající ze 16 položek. Před TPSRS, každý dobrovolník podstoupil školení k dokončení stupnice., Subjekty byly požádány, aby označily bod, který identifikoval jeho současný subjektivní stav na přímce 100 mm umístěné mezi dvěma slovy, která popisují opačné stavy nálady(např. Faktoriální analýza portugalské verze stupnice identifikovala čtyři faktory (Zuardi et al.,, 1993): (1) „úzkost“, zahrnující položky v klidu–vzrušený, uvolněný–napjatý a klidný–ustaraný; (2) „sedace“, včetně položek alert–ospalý a pozorný–zasněný; (3) „kognitivní porucha“, včetně quick-witted–mentálně pomalý, zdatný–nekompetentní, energický–letargický, s jasnou hlavou-muzzy, gregarious–stažený, dobře koordinovaný–nemotorný a silný-slabý; a (4) „nepohodlí“, “ včetně položek, které se zajímají–znuděný, šťastný–smutný, spokojený–nespokojený a přátelský–antagonistický (Parente et al., 2005). Od předchozích studií s oběma anxiogenními (Crippa et al., 2004; Parente et al.,, 2005) a anxiolytické léky včetně CBD (Crippa et al., 2004, 2011; Bergamaschi et al., 2011a) ukázaly, že pouze úzkost a sedace faktory přítomny změny během mluvení na veřejnosti úkolů, použili jsme pouze položky, které z těchto faktorů VAMS snížit administrativní čas a umožnit provedení protokolu. Tento postup byl dříve použit ve validační studii PSRST (Zuardi et al., 2013).
Fyziologické Měření
Systolický krevní tlak, DBP, a srdeční frekvence (HR) byly měřeny s digitální tlakoměr (Omron, Brazílie).,
test veřejného mluvení v reálné situaci (TPSRS)
v tomto postupu musí každý subjekt mluvit před skupinou a ve stejné experimentální relaci se účastnit publika, když mluví ostatní členové skupiny. Publikum je instruováno, aby během projevů mlčelo as neutrálním výrazem.
bylo provedeno pět experimentálních sezení s 12 subjekty (kromě 1, které zahrnovaly 11 subjektů). Na začátku zasedání byli dobrovolníci informováni o počtu léčby, kterou obdrží (jak je uvedeno výše)., Dobrovolníci byli poté instruováni, aby obsadili místa označená jejich příslušnými čísly léčby. Sedadla byla očíslována tak, že na konci pěti zasedání obsadili subjekty každé léčebné skupiny všechny možné pozice. Sekvence postupů vždy sledovala stejné pořadí od prvního do dvanáctého křesla ve snaze minimalizovat možný účinek pořadí v pořadí reproduktorů., Například, předměty v CBD-300 skupině obsadili následující pozice: první sezení – 3, 8; druhé zasedání – 4, 9; třetí sezení – 5, 10, čtvrté zasedání – 1, 6, 11, páté zasedání – 2, 7, 12.
Postup
Dobrovolníci začala experimentální sezení po alespoň 6 hodin spánku a 2 h po jídle standardní snídaní (200 ml čokoládového mléka a 100 g chleba s margarínem).,
12 dobrovolníků sedělo v židlích uspořádaných v půlkruhu, po předem stanoveném pořadí podle čísla léčby přiřazeného každému z nich a provedlo základní měření, následované příjmem pěti tobolek v intervalu 5 minut pro každého dobrovolníka. Tato fáze byla dokončena po dobu 1 h. dobrovolníci pak sledovali film o ptácích Amazonského lesa trvající asi 20 min. Poté se měření opakovala s intervalem 5 min pro každý subjekt (předběžné opatření)., 2 h a 20 min poté, co první dobrovolník dostal léčbu, všichni sledovali video trvající asi 10 min se zaznamenanými pokyny pro řečový test. 2 hodiny a 30 minut poté, co první dobrovolník obdržel léčbu, začali provádět řečový test, který trval 5 minut. Následně byli ostatní dobrovolníci podrobeni řečovému testu ve stejném pořadí, v jakém byli léčeni., Řeč test se skládal z tiše připravuje 1-min řeči na téma týkající se „podmínky jedné veřejné služby vašeho města,“ vybráno náhodou z 12 možností, a odhalil okamžitě, před řeči přípravy. Připravený projev byl poté prezentován na 2 min, přičemž ostatní účastníci a vyšetřovatelé sloužili jako publikum. Řeč byla přerušena v polovině měření., Sekvence postupů v této fázi byla následující: (A) sezení na židli uspořádané před ostatními; (b) výběr řečového tématu; (c) přemýšlení o tématu po dobu 1 min; (d) zahájení řeči, která byla přerušena po 1 min; (e) dokončení stupnice sebehodnocení (faktory úzkosti a sedace vas) a fyziologická měření; (f) pokračování řeči další minutu. Tato sekvence trvala maximálně 5 minut, takže po 1 hodině všichni dobrovolníci prošli postupem. Konečná fáze studie začala 216 min poté, co první dobrovolník vzal drogu., Všechna měření byla opakována a udržovala 5minutový interval pro každého dobrovolníka. Tabulka 1 představuje nástin experimentálního postupu.

tabulka 1. Harmonogram experimentální relace.
Statistická analýza
klinické a demografické charakteristiky byly analyzovány neparametrickými testy (pohlaví) a jednofaktorovou analýzou rozptylu (ANOVA; věk, BMI a STAI-trait).,
skóre ve dvou faktorech vam, arteriálním systolickém a diastolickém tlaku a srdeční frekvenci bylo analyzováno pomocí analýzy rozptylu opakovaných měření (opakovaná měření ANOVA)včetně fáze faktorů, skupin a interakce fázové skupiny. V případech, kdy nebyly dosaženy podmínky sféričnosti, byly stupně volnosti opakovaného faktoru korigovány epsilonem Huynh-Feldt. Srovnání mezi skupinami byly v každé fázi pomocí jedno-faktorová ANOVA následované více srovnání s Student-Newman-Keuls testu.,
analýza dat byla provedena pomocí statistického balíčku pro verzi 17 Social Sciences (SPSS) a přijatá úroveň významnosti byla p < 0.05.
výsledky
demografické a klinické charakteristiky subjektů jsou uvedeny v tabulce 2. Skupiny se výrazně nelišily ve vztahu k pohlaví, věku, BMI a skóre STAI-trait.

tabulka 2. Demografická a klinická charakteristika skupin.,
opakovaná měření ANOVA skóre v úzkostném faktoru vas vykazovala významný účinek fáze (F3,162 = 60, 24; p<0,001), skupina (F4,54 = 3, 25; p = 0, 018) a interakce fázové skupiny (F4, 54 = 3, 25; p=0, 018) a interakce fázové skupiny (F12, 162 = 3,79; p< 0,001, obrázek 1A). Post hoc srovnání mezi skupinami v každé fázi ukázaly významné rozdíly (p < 0.05) mezi PLAC a CLON na řeč a post-stres fází., Skóre CBD-300 skupině byly výrazně odlišné od těch, CBD-900 skupina na projev fáze a od těch PLAC a CBD-100 skupin během post-stres fáze (p < 0.05). Na obrázku 1b je znázorněna obrácená křivka dávkové odezvy ve tvaru písmene U indukovaná CBD v post-stresové fázi. Pokud jde o sedační faktor vas, opakovaná opatření ANOVA vykazovala významné účinky fáze (F2,16, 116, 7 = 3, 11; p = 0, 028) a skupiny (F4, 54 = 3, 48; p = 0, 013, obrázek 2A)., Obecné post hoc srovnání mezi skupinami ukázalo, že klonazepam vyvolal vyšší sedativní účinek ve srovnání s ostatními skupinami (hlavní účinek léčby). Podobný účinek byl pozorován v post-stresové fázi (p < 0, 05).
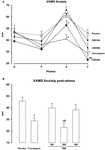
obrázek 1. Změny ve skóre úzkosti faktor Vizuální Analogová Náladu Měřítku (VAMS) (mm) vyvolané mluvení na veřejnosti u zdravých dobrovolníků (A) během na počátku (B) a během pre-stres (P), řeči (S) a post-stres (F) fáze (A)., Pro přehlednost jsou výsledky z poslední fáze (F) zobrazeny také jako sloupcový graf (B). Body představují prostředky ± SEM 11-12 subjektů. Hvězdičky ( ∗ ) ukazují statisticky významné rozdíly ve srovnání se skupinou placeba, ( + ) ukazuje významný rozdíl ve srovnání se skupinou CBD-900 a (&) ukazuje významný rozdíl ve srovnání se skupinou CBD-100.
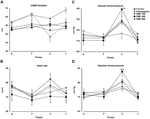
OBRÁZEK 2., Změny v sedaci faktor VAMS (mm), srdeční frekvence , systolický (C) a diastolický (D) krevní tlak (mm Hg) vyvolané mluvení na veřejnosti u zdravých dobrovolníků. Body představují prostředky ± SEM 11-12 subjektů. Hvězdičky ( ∗ ) ukazují statisticky významné rozdíly ve srovnání s ostatními skupinami, (&) znamená významný rozdíl ve srovnání s klonazepamem a ( $ ) znamená významný rozdíl ve srovnání se skupinou CBD-100.,
Diskuse
Jsme použili TPSRS experimentálně vyvolat úzkost a zkoumali, zda anxiolyticky CBD v lidech vytváří obrácené U-tvaru křivky dávka-odezva. V souladu s předchozími důkazy (Zuardi et al., 2013), tento protokol významně zvýšil Subjektivní úzkost, krevní tlak a srdeční frekvenci, jak ukazuje významný účinek fáze nalezené v opakovaném měření ANOVA., Kromě toho byla tpsrs citlivá při detekci anxiolytického účinku klonazepamu, známého anxiolytického léčiva, což naznačuje, že může být použita k identifikaci potenciálně anxiolytických léků.
v dávce 300 mg CBD významně snížila Subjektivní úzkost ve srovnání se skupinou PLAC během post-řečové fáze protokolu. Totéž však neplatilo pro nižší (100 mg) nebo vyšší (900 mg) dávku léku., Subjektivní úzkostné skóre skupiny CBD-300 se navíc výrazně lišilo od skóre skupiny CBD-900 během fáze řeči a od skupiny CBD-100 během post-řečové fáze. Tyto výsledky naznačují, že akutní anxiolyticky CBD následoval obráceného U-tvar křivky dávka-odezva, což je v souladu s výsledky ze studií na zvířatech (Guimarães et al., 1990; Levin et al., 2014; Nazario et al., 2015; Peres et al., 2016). Je zajímavé, že stejná dávka CBD, která vyvolala anxiolytické účinky (300 mg), nesnížila systolický a DBP jako klonazepam., Tato disociace mezi anxiolytika a sympathoinhibitory účinky po akutním podání CBD je v souladu s naším pozorováním pomocí SPST u zdravých dobrovolníků (Zuardi et al., 1993) a u pacientů se sociální fobií (Bergamaschi et al., 2011a).
mechanismus, který je základem tohoto vzorce účinku CBD na odpověď na dávku, nelze dosud plně vysvětlit. U lidí se zdá, že limbické a paralimbické oblasti mozku se podílejí na anxiolytickém působení CBD., Například studie využívající jednofotonovou emisní počítačovou tomografii (SPECT) u zdravých dobrovolníků a pacientů s léčivou látkou se SAD prokázaly zapojení stejných oblastí zapojených do anxiolytického účinku CBD 400 mg, jmenovitě levého parahippocampálního gyru a levého komplexu amygdala-hippocampus (Crippa et al., 2004, 2011). Pomocí funkčního zobrazování magnetickou rezonancí (fMRI) u zdravých dobrovolníků vědci zjistili, že CBD 600 mg oslabená aktivace v amygdale a přední kůře cingulate během rozpoznávání strašných výrazů obličeje (Fusar-Poli et al., 2009)., Autoři dále vysvětlili, že tato akce CBD byla zprostředkována změnami subkortikální prefrontální konektivity prostřednictvím amygdaly a přední cingulární kůry (Fusar-Poli et al., 2010).
navzdory identifikaci oblastí mozku, které se mohou podílet na anxiolytickém účinku CBD, zůstává objasněn specifický farmakologický mechanismus zodpovědný za tento účinek., CBD je lék s více farmakologickými cíli, včetně interakce s několika receptory (CB1, CB2, GPR55, TRPV1 a 5-HT1A), interference s příjmem a metabolismem endokanabinoidů a zvýšení hipokampální neurogeneze v dospělém mozku (Zuardi et al., 2017). Několik studií podpořilo zapojení receptorů 5-HT1A do akutního anxiolytického účinku CBD., Například, anxiolyticky vyvolané systémové nebo uvnitř hřbetní periaqueductal šedá (DPAG) injekce CBD u potkanů je zabráněno tím, že 5-HT1A receptorů (Campos a Guimarães, 2008; Soares et al., 2010). Podobná interakce mezi receptory CBD a 5-HT1A v jiných mozkových strukturách souvisejících s kontrolou úzkostného chování, jako je jádro lůžka stria terminallis nebo předběžná čelní kůra, se také podílí na útlumu úzkostných odpovědí (Gomes et al., 2011, 2012; Fogaça et al., 2014)., V kultivovaných buňkách bylo hlášeno, že CBD působí jako agonista receptoru 5-HT1A (Russo et al., 2005), ačkoli nedávné studie naznačují, že tomu tak není v podmínkách plátků nebo in vivo. Zdá se, že usnadnění neurotransmise zprostředkované 5-HT1A CBD nezahrnuje blokádu zpětného vychytávání 5-HT nebo změny exprese 5-HT1A mRNA v DPAG po chronickém podání CBD (Campos et al., 2013). Tato pozorování naznačují, že modulace receptorů 5-HT1A CBD je složitá a může zahrnovat alosterické interakce (Rock et al., 2011).,
jak již bylo zmíněno dříve, mechanismy odpovědné za obrácenou křivku dávkové odpovědi CBD ve tvaru písmene U jsou špatně pochopeny. Mohly by zahrnovat interakce s vanilloidním receptorem 1 nebo TRPV1. Při vysokých koncentracích může CBD tyto receptory aktivovat a usnadnit uvolňování glutamátu a obranné reakce (Guimarães et al., 1991; Campos and Guimarães, 2009). Tento mechanismus by mohl maskovat anxiolytický účinek CBD zprostředkovaný receptory 5-HT1A., Testování tuto možnost pomocí intra-DPAG injekce u potkanů, Campos a Guimarães (2009) ukázal, že předčištění s TRPV1 antagonista (capsazepine) se obrátil vyšší a neefektivní dávkou CBD do anxiolytikum. Zbývá testovat, zda se podobný mechanismus podílí také na křivce dávkové odpovědi ve tvaru písmene U pozorované v naší studii. V souladu s předchozími důkazy, které naznačují, že CBD má slabší sedativní vlastnosti ve srovnání s benzodiazepiny (Zuardi et al., 1993), anxiolytická dávka CBD (300 mg) vyvolala výrazně nižší hladinu sedace než klonazepam., Je to výhoda, kterou je třeba zdůraznit, protože poškození sedace a motorické koordinace patří mezi nejčastější nežádoucí účinky benzodiazepinů, kromě potenciální závislosti, kognitivních deficitů a abstinenčních příznaků, zejména ve stáří (Sgnaolin et al., 2016). Tyto nežádoucí účinky nebyly pozorovány při použití CBD (Bergamaschi et al., 2011b).
zde uvedené nálezy je třeba interpretovat opatrně, vzhledem k omezením naší studie., Za prvé, bylo by žádoucí, aby měření plazmatické hladiny CBD a clonazepam a vztah těchto měření rozsahu úrovně úzkosti; bez křivku dávka-odpověď, přetrvávají pochybnosti o tom, zda účinky CBD vlastně to sledovat obrácené U-křivce ve tvaru. Je však třeba poznamenat, že předchozí vyšetření nebyla schopna navázat přímý vztah mezi plazmatickými hladinami CBD a jeho klinickými účinky (Agurell et al., 1986). Malá velikost vzorku navíc omezuje statistickou sílu studie., Také návrh studie nám neumožňuje vyloučit možnost, že další mírná dávka (např. 400 nebo 600 mg) mohla mít ještě větší anxiolytické účinky. Například předchozí studie prokázaly akutní anxiolytické účinky 400 mg CBD ve studiích SPECT u zdravých dobrovolníků (Crippa et al., 2004) a u pacientů se sociální fobií (Crippa et al., 2011) a CBD 600 mg v experimentu fMRI se zdravými muži (Bhattacharyya et al., 2010)., Ačkoli to není nutné pro tento důkaz koncepční studie, tato omezení by mohla být překonána v budoucích studiích zkoumajících další 2-3 dávky mezi 300 a 900 mg, aby se vytvořil skutečný terapeutický index.
Závěr
Naše výsledky jsou v souladu s důkazy z preklinických studií a podporují názor, že CBD vyvolává akutní anxiolytické účinky s obráceného U-tvar křivky dávka-odezva u lidí. Tato zjištění zdůrazňují důležitost pečlivého výběru rozsahů dávek při zkoumání potenciálních terapeutických účinků CBD., Další studie hodnotící křivku dávkové odpovědi CBD v jiných podmínkách, jako je schizofrenie, bolest, epilepsie a Parkinsonova choroba a zahrnující chronické podávání CBD, jsou nezbytné k převedení předklinických důkazů do klinické praxe a ke stanovení přesného terapeutického okna CBD pro každý stav.
autorské příspěvky
az, JH a JC navrhli studii. Nr, AS a SB provedly experimenty. AZ a FG provedly statistickou analýzu. AZ napsal první návrh rukopisu., Všichni autoři přispěli a schválili konečný rukopis.
Střet Zájmů Prohlášení
AZ, JH, FG, a JC jsou co-vynálezce (Mechoulam R, JC, Guimaraes FS, AZ, JH, Breuer A) patent „Fluorované CBD sloučeniny, kompozice a jejich použití. Hospoda. Č.: WO / 2014 / 108899. Mezinárodní Přihláška Č.: PCT/IL2014 / 050023 “ Def. My ne. Reg. 62193296; 29/07/2015; INPI dne 19/08/2015 (BR1120150164927). Univerzita v São Paulu licencovala patent na Phytecs Pharm (USP rezoluce č. 15.1.130002.1.1)., Univerzita v São Paulu má dohodu s Prati-Donaduzzi (Toledo, Brazílie) o „vývoji farmaceutického přípravku obsahujícího syntetický kanabidiol a prokázání jeho bezpečnosti a terapeutické účinnosti při léčbě epilepsie, schizofrenie, Parkinsonovy choroby a úzkostných poruch.“JH a JC získaly podporu Cestování od společnosti BSPG-Pharm.
ostatní autoři prohlašují, že výzkum byl proveden bez jakýchkoli obchodních nebo finančních vztahů, které by mohly být chápány jako potenciální střet zájmů.,
recenzenti RWG, KA a manipulační Editor prohlásil jejich společná příslušnost a manipulaci Editor uvádí, že proces však splněny normy pro spravedlivé a objektivní recenzi.
potvrzení
AZ, JH, FG a JC jsou příjemci fellowship award od Conselho Nacional de Desenvolvimento cientifico e Tecnológico (CNPq, Brazílie). Tato studie byla podpořena grantem CNPq (CNPq / MS / SCTIE / DECIT N∘ 26/2014-Pesquisas sobre Distúrbios Neuropsiquiátricos; 466805/2014-4) a bspg-Pharm (Sandwich, UK) laskavě dodala CBD bez nákladů.,
Campos, a. C., a Guimarães, F. S. (2008). Zapojení receptorů 5ht1a do anxiolytických účinků kanabidiolu injikovaného do dorsolaterální periaqueduktální šedé potkanů. Psychofarmakologie (Berl) 199, 223-230. doi: 10.1007/s00213-008-1168-x
PubMed Abstraktní | CrossRef Plný Text | Google Scholar
Campos, a. C., a Guimarães, F. S. (2009). Důkazy o potenciální roli receptorů TRPV1 v dorsolaterální periaqueduktální šedé v útlumu anxiolytických účinků kanabinoidů. Pořada., Neuropsychopharmacol. Biol. Psychiatry 33, 1517–1521. doi: 10.1016/j.pnpbp.2009.08.017
PubMed Abstract | CrossRef Full Text | Google Scholar